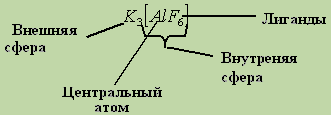
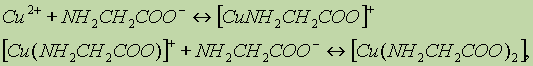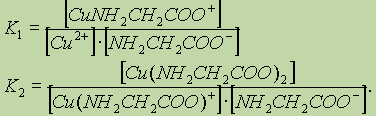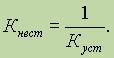▌ļÕĻ“ŅĒĒÓ ßĶßļĶŅ“ÕĻÓ
ąÜąŠą╝ą┐ą╗ąĄą║čüąŠąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄ
ą×ąĪąØą×ąÆą½ ąóąĢą×ąĀąĢąóąśą¦ąĢąĪąÜą×ąÖ ąźąśą£ąśąś9. ąÜąŠą╝ą┐ą╗ąĄą║čüąŠąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄąÆą┐ąĄčĆą▓čŗąĄ ą┐ąŠąĮčÅčéąĖąĄ ąŠ ą║ąŠą╝ą┐ą╗ąĄą║čüąĄ, ą║ą░ą║ ąŠ čüą╗ąŠąČąĮąŠą╣ čćą░čüčéąĖčåąĄ, čüąŠčüč鹊čÅčēąĄą╣ ąĖčģ ą▓ąĮčāčéčĆąĄąĮąĮąĄą╣ ąĖ ą▓ąĮąĄčłąĮąĄą╣ čüč乥čĆčŗ, ą▒čŗą╗ąŠ ą▓ą▓ąĄą┤ąĄąĮąŠ ąÉ. ąÆąĄčĆąĮąĄčĆąŠą╝ ą▓ 1892 ą│ąŠą┤čā. ąĪąŠą│ą╗ą░čüąĮąŠ čŹč鹊ą╝čā ąŠą┐čĆąĄą┤ąĄą╗ąĄąĮąĖčÄ, ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮčŗąĄ (ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗąĄ) čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ŌĆō čŹč鹊 čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ, čüčāčēąĄčüčéą▓čāčÄčēąĖąĄ ą║ą░ą║ ą▓ ą║čĆąĖčüčéą░ą╗ą╗ąĖč湥čüą║ąŠą╝ čüąŠčüč鹊čÅąĮąĖąĖ, čéą░ą║ ąĖ ą▓ čĆą░čüčéą▓ąŠčĆą░čģ, ąŠčüąŠą▒ąĄąĮąĮąŠčüčéčÅą╝ąĖ ą║ąŠč鹊čĆčŗčģ čÅą▓ą╗čÅčÄčéčüčÅ ąĮą░ą╗ąĖčćąĖąĄ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ąĖąŠąĮą░ ąĖą╗ąĖ ą░č鹊ą╝ą░-ą░ą║čåąĄą┐č鹊čĆą░ 菹╗ąĄą║čéčĆąŠąĮąŠą▓, ąŠą║čĆčāąČąĄąĮąĮąŠą│ąŠ ą╗ąĖą│ą░ąĮą┤ą░ą╝ąĖ-ą┤ąŠąĮąŠčĆą░ą╝ąĖ 菹╗ąĄą║čéčĆąŠąĮąŠą▓. ąøąĖą│ą░ąĮą┤čŗ čüą┐ąŠčüąŠą▒ąĮčŗ ąŠčéčēąĄą┐ą╗čÅčéčīčüčÅ ąŠčé čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ ą┐ąŠ ą│ąĄč鹥čĆąŠą╗ąĖčéąĖč湥čüą║ąŠą╝čā čéąĖą┐čā (čéą░ą║ ą┐ąŠą┤č湥čĆą║ąĖą▓ą░ąĄčéčüčÅ ą░ą║čåąĄą┐č鹊čĆąĮčŗą╣ čģą░čĆą░ą║č鹥čĆ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ ąĖ ą┤ąŠąĮąŠčĆąĮčŗą╣ čģą░čĆą░ą║č鹥čĆ ą╗ąĖą│ą░ąĮą┤ąŠą▓, čģąŠčéčÅ ąĮąĄ ąĖčüą║ą╗čÄč湥ąĮ ąĖ čé. ąĮą░ąĘ. p -ą┤ąŠąĮąŠčĆąĮčŗą╣ čģą░čĆą░ą║č鹥čĆ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ ąĖ p -ą░ą║čåąĄą┐č鹊čĆąĮčŗą╣ čģą░čĆą░ą║č鹥čĆ ą╗ąĖą│ą░ąĮą┤ąŠą▓). ąøąĖą│ą░ąĮą┤ą░ą╝ąĖ ą╝ąŠą│čāčé ą▒čŗčéčī ąĖąŠąĮčŗ ąĖą╗ąĖ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╝ąŠą╗ąĄą║čāą╗čŗ, ąŠą┐čĆąĄą┤ąĄą╗ąĄąĮąĮčŗą╝ ąŠą▒čĆą░ąĘąŠą╝ čĆą░čüą┐ąŠą╗ąŠąČąĄąĮąĮčŗąĄ ą▓ąŠą║čĆčāą│ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░. ąøąĖą│ą░ąĮą┤čŗ čģą░čĆą░ą║č鹥čĆąĖąĘčāčÄčéčüčÅ ąĮą░ą╗ąĖčćąĖąĄą╝: 1) ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ - ąĮčāą║ą╗ąĄąŠčäąĖą╗čīąĮčŗčģ ą░č鹊ą╝ąŠą▓, čüą┐ąŠčüąŠą▒ąĮčŗčģ čāčćą░čüčéą▓ąŠą▓ą░čéčī ą▓ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąĖ (ą║ čéą░ą║ąĖą╝ čåąĄąĮčéčĆą░ą╝ ąŠčéąĮąŠčüčÅčéčüčÅ ąĖ ąĮąĄąĮą░čüčŗčēąĄąĮąĮčŗąĄ ą│čĆčāą┐ą┐ąĖčĆąŠą▓ą║ąĖ ą░č鹊ą╝ąŠą▓); 2) ą┤ąĄąĮčéą░čéąĮąŠčüčéčīčÄ ŌĆō ą║ąŠą╗ąĖč湥čüčéą▓ąŠą╝ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ ą╗ąĖą│ą░ąĮą┤ą░, ą║ąŠč鹊čĆčŗąĄ čāčćą░čüčéą▓čāčÄčé ą▓ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąĖ (ą▓ čŹč鹊ą╣ čüą▓čÅąĘąĖ čĆą░ąĘą╗ąĖčćą░čÄčé ą╝ąŠąĮąŠ- ąĖ ą┐ąŠą╗ąĖą┤ąĄąĮčéą░čéąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ).
ąøąĖą│ą░ąĮą┤čŗ čģą░čĆą░ą║č鹥čĆąĖąĘčāčÄčéčüčÅ ąĮą░ą╗ąĖčćąĖąĄą╝: 1) ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ - ąĮčāą║ą╗ąĄąŠčäąĖą╗čīąĮčŗčģ ą░č鹊ą╝ąŠą▓, čüą┐ąŠčüąŠą▒ąĮčŗčģ čāčćą░čüčéą▓ąŠą▓ą░čéčī ą▓ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąĖ (ą║ čéą░ą║ąĖą╝ čåąĄąĮčéčĆą░ą╝ ąŠčéąĮąŠčüčÅčéčüčÅ ąĖ ąĮąĄąĮą░čüčŗčēąĄąĮąĮčŗąĄ ą│čĆčāą┐ą┐ąĖčĆąŠą▓ą║ąĖ ą░č鹊ą╝ąŠą▓); 2) ą┤ąĄąĮčéą░čéąĮąŠčüčéčīčÄ ŌĆō ą║ąŠą╗ąĖč湥čüčéą▓ąŠą╝ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ ą╗ąĖą│ą░ąĮą┤ą░, ą║ąŠč鹊čĆčŗąĄ čāčćą░čüčéą▓čāčÄčé ą▓ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąĖ (ą▓ čŹč鹊ą╣ čüą▓čÅąĘąĖ čĆą░ąĘą╗ąĖčćą░čÄčé ą╝ąŠąĮąŠ- ąĖ ą┐ąŠą╗ąĖą┤ąĄąĮčéą░čéąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ).ąÆ ą║ą░č湥čüčéą▓ąĄ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ čćą░čēąĄ ą▓čüąĄą│ąŠ ą▓čŗčüčéčāą┐ą░čÄčé 菹╗ąĄą╝ąĄąĮčéčŗ ą│ą╗ą░ą▓ąĮčŗčģ ą┐ąŠą┤ą│čĆčāą┐ą┐: VA: N, P, As; VIA: O, S, Se; VIIA: F- , Cl- , Br- , I- , ą░ čéą░ą║ąČąĄ ąĮąĄą┐čĆąĄą┤ąĄą╗čīąĮčŗąĄ, ą░čĆąŠą╝ą░čéąĖč湥čüą║ąĖąĄ ąĖ ą│ąĄč鹥čĆąŠčåąĖą║ą╗ąĖč湥čüą║ąĖąĄ čāą│ą╗ąĄą▓ąŠą┤ąŠčĆąŠą┤čŗ.ąÜ ą╝ąŠąĮąŠą┤ąĄąĮčéą░čéąĮčŗą╝ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ąŠčéąĮąŠčüčÅčéčüčÅ ą│ą░ą╗ąŠą│ąĄąĮąĖą┤-ąĖąŠąĮčŗ, ą┤čĆčāčģą░č鹊ą╝ąĮčŗąĄ ą╝ąŠą╗ąĄą║čāą╗čŗ O2, N2, N2, ą░ čéą░ą║ąČąĄ čĆčÅą┤ čüą╗ąŠąČąĮčŗčģ ą░čĆąŠą╝ą░čéąĖč湥čüą║ąĖčģ ą│ąĄč鹥čĆąŠčüąŠąĄą┤ąĖąĮąĄąĮąĖą╣. ąóąĖą┐ąĖčćąĮčŗą╝ ą┐čĆąĖą╝ąĄčĆąŠą╝ ą┐ąŠą╗ąĖą┤ąĄąĮčéą░čéąĮąŠą│ąŠ ą╗ąĖą│ą░ąĮą┤ą░ ą╝ąŠąČąĄčé čüą╗čāąČąĖčéčī ąŁąöąóąÉ (čŹčéąĖą╗ąĄąĮą┤ąĖą░ą╝ąĖąĮč鹥čéčĆą░čåąĄčéą░čé). ąØąĄąŠą▒čģąŠą┤ąĖą╝ąŠ ąĖą╝ąĄčéčī ą▓ ą▓ąĖą┤čā, čćč鹊 ą║ąŠą╗ąĖč湥čüčéą▓ąŠ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ ąĖ ą┤ąĄąĮčéą░čéąĮąŠčüčéčī ąĮąĄ ą▓čüąĄą│ą┤ą░ čüąŠą▓ą┐ą░ą┤ą░čÄčé.
ąÜą╗ą░čüčüąĖčäąĖą║ą░čåąĖčÅ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗčģ čüąŠąĄą┤ąĖąĮąĄąĮąĖą╣.
ą¤ąŠ ąĘą░čĆčÅą┤čā ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ ąĖąŠąĮą░:
ą░) ą║ą░čéąĖąŠąĮąĮčŗąĄ: 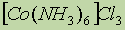 - ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
- ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
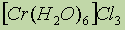 - ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 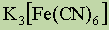 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
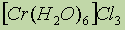 - ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 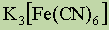 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 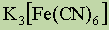 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).ą▓) ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
) ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ: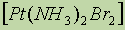 - ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
ą¤ąŠ ą┐čĆąĖčĆąŠą┤ąĄ ą╗ąĖą│ą░ąĮą┤ą░:
ą░) čü ąĮąĄą╣čéčĆą░ą╗čīąĮčŗą╝ąĖ ą╗ąĖą│ą░ąĮą┤ą░ą╝ąĖ: 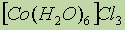 - ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
- ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.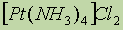 - č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
- č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
ąøąĖą│ą░ąĮą┤ą░ą╝ąĖ ą╝ąŠą│čāčé ą▒čŗčéčī ąĖąŠąĮčŗ ąĖą╗ąĖ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╝ąŠą╗ąĄą║čāą╗čŗ, ąŠą┐čĆąĄą┤ąĄą╗ąĄąĮąĮčŗą╝ ąŠą▒čĆą░ąĘąŠą╝ čĆą░čüą┐ąŠą╗ąŠąČąĄąĮąĮčŗąĄ ą▓ąŠą║čĆčāą│ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░. ąøąĖą│ą░ąĮą┤čŗ čģą░čĆą░ą║č鹥čĆąĖąĘčāčÄčéčüčÅ ąĮą░ą╗ąĖčćąĖąĄą╝: 1) ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ - ąĮčāą║ą╗ąĄąŠčäąĖą╗čīąĮčŗčģ ą░č鹊ą╝ąŠą▓, čüą┐ąŠčüąŠą▒ąĮčŗčģ čāčćą░čüčéą▓ąŠą▓ą░čéčī ą▓ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąĖ (ą║ čéą░ą║ąĖą╝ čåąĄąĮčéčĆą░ą╝ ąŠčéąĮąŠčüčÅčéčüčÅ ąĖ ąĮąĄąĮą░čüčŗčēąĄąĮąĮčŗąĄ ą│čĆčāą┐ą┐ąĖčĆąŠą▓ą║ąĖ ą░č鹊ą╝ąŠą▓); 2) ą┤ąĄąĮčéą░čéąĮąŠčüčéčīčÄ ŌĆō ą║ąŠą╗ąĖč湥čüčéą▓ąŠą╝ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ ą╗ąĖą│ą░ąĮą┤ą░, ą║ąŠč鹊čĆčŗąĄ čāčćą░čüčéą▓čāčÄčé ą▓ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąĖ (ą▓ čŹč鹊ą╣ čüą▓čÅąĘąĖ čĆą░ąĘą╗ąĖčćą░čÄčé ą╝ąŠąĮąŠ- ąĖ ą┐ąŠą╗ąĖą┤ąĄąĮčéą░čéąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ).
ąøąĖą│ą░ąĮą┤čŗ čģą░čĆą░ą║č鹥čĆąĖąĘčāčÄčéčüčÅ ąĮą░ą╗ąĖčćąĖąĄą╝: 1) ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ - ąĮčāą║ą╗ąĄąŠčäąĖą╗čīąĮčŗčģ ą░č鹊ą╝ąŠą▓, čüą┐ąŠčüąŠą▒ąĮčŗčģ čāčćą░čüčéą▓ąŠą▓ą░čéčī ą▓ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąĖ (ą║ čéą░ą║ąĖą╝ čåąĄąĮčéčĆą░ą╝ ąŠčéąĮąŠčüčÅčéčüčÅ ąĖ ąĮąĄąĮą░čüčŗčēąĄąĮąĮčŗąĄ ą│čĆčāą┐ą┐ąĖčĆąŠą▓ą║ąĖ ą░č鹊ą╝ąŠą▓); 2) ą┤ąĄąĮčéą░čéąĮąŠčüčéčīčÄ ŌĆō ą║ąŠą╗ąĖč湥čüčéą▓ąŠą╝ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ ą╗ąĖą│ą░ąĮą┤ą░, ą║ąŠč鹊čĆčŗąĄ čāčćą░čüčéą▓čāčÄčé ą▓ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąĖ (ą▓ čŹč鹊ą╣ čüą▓čÅąĘąĖ čĆą░ąĘą╗ąĖčćą░čÄčé ą╝ąŠąĮąŠ- ąĖ ą┐ąŠą╗ąĖą┤ąĄąĮčéą░čéąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ).ąÆ ą║ą░č湥čüčéą▓ąĄ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ čćą░čēąĄ ą▓čüąĄą│ąŠ ą▓čŗčüčéčāą┐ą░čÄčé 菹╗ąĄą╝ąĄąĮčéčŗ ą│ą╗ą░ą▓ąĮčŗčģ ą┐ąŠą┤ą│čĆčāą┐ą┐: VA: N, P, As; VIA: O, S, Se; VIIA: F- , Cl- , Br- , I- , ą░ čéą░ą║ąČąĄ ąĮąĄą┐čĆąĄą┤ąĄą╗čīąĮčŗąĄ, ą░čĆąŠą╝ą░čéąĖč湥čüą║ąĖąĄ ąĖ ą│ąĄč鹥čĆąŠčåąĖą║ą╗ąĖč湥čüą║ąĖąĄ čāą│ą╗ąĄą▓ąŠą┤ąŠčĆąŠą┤čŗ.ąÜ ą╝ąŠąĮąŠą┤ąĄąĮčéą░čéąĮčŗą╝ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ąŠčéąĮąŠčüčÅčéčüčÅ ą│ą░ą╗ąŠą│ąĄąĮąĖą┤-ąĖąŠąĮčŗ, ą┤čĆčāčģą░č鹊ą╝ąĮčŗąĄ ą╝ąŠą╗ąĄą║čāą╗čŗ O2, N2, N2, ą░ čéą░ą║ąČąĄ čĆčÅą┤ čüą╗ąŠąČąĮčŗčģ ą░čĆąŠą╝ą░čéąĖč湥čüą║ąĖčģ ą│ąĄč鹥čĆąŠčüąŠąĄą┤ąĖąĮąĄąĮąĖą╣. ąóąĖą┐ąĖčćąĮčŗą╝ ą┐čĆąĖą╝ąĄčĆąŠą╝ ą┐ąŠą╗ąĖą┤ąĄąĮčéą░čéąĮąŠą│ąŠ ą╗ąĖą│ą░ąĮą┤ą░ ą╝ąŠąČąĄčé čüą╗čāąČąĖčéčī ąŁąöąóąÉ (čŹčéąĖą╗ąĄąĮą┤ąĖą░ą╝ąĖąĮč鹥čéčĆą░čåąĄčéą░čé). ąØąĄąŠą▒čģąŠą┤ąĖą╝ąŠ ąĖą╝ąĄčéčī ą▓ ą▓ąĖą┤čā, čćč鹊 ą║ąŠą╗ąĖč湥čüčéą▓ąŠ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ ąĖ ą┤ąĄąĮčéą░čéąĮąŠčüčéčī ąĮąĄ ą▓čüąĄą│ą┤ą░ čüąŠą▓ą┐ą░ą┤ą░čÄčé.

ąÜą╗ą░čüčüąĖčäąĖą║ą░čåąĖčÅ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗčģ čüąŠąĄą┤ąĖąĮąĄąĮąĖą╣.
ą¤ąŠ ąĘą░čĆčÅą┤čā ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ ąĖąŠąĮą░:
ą░) ą║ą░čéąĖąŠąĮąĮčŗąĄ: 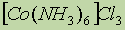 - ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
- ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
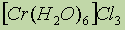 - ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 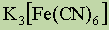 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
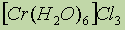 - ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 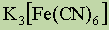 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 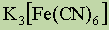 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).ą▓) ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
) ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ: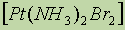 - ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
ą¤ąŠ ą┐čĆąĖčĆąŠą┤ąĄ ą╗ąĖą│ą░ąĮą┤ą░:
ą░) čü ąĮąĄą╣čéčĆą░ą╗čīąĮčŗą╝ąĖ ą╗ąĖą│ą░ąĮą┤ą░ą╝ąĖ: 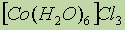 - ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
- ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.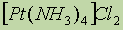 - č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
- č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
ąÜ ą╝ąŠąĮąŠą┤ąĄąĮčéą░čéąĮčŗą╝ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ąŠčéąĮąŠčüčÅčéčüčÅ ą│ą░ą╗ąŠą│ąĄąĮąĖą┤-ąĖąŠąĮčŗ, ą┤čĆčāčģą░č鹊ą╝ąĮčŗąĄ ą╝ąŠą╗ąĄą║čāą╗čŗ O2, N2, N2, ą░ čéą░ą║ąČąĄ čĆčÅą┤ čüą╗ąŠąČąĮčŗčģ ą░čĆąŠą╝ą░čéąĖč湥čüą║ąĖčģ ą│ąĄč鹥čĆąŠčüąŠąĄą┤ąĖąĮąĄąĮąĖą╣. ąóąĖą┐ąĖčćąĮčŗą╝ ą┐čĆąĖą╝ąĄčĆąŠą╝ ą┐ąŠą╗ąĖą┤ąĄąĮčéą░čéąĮąŠą│ąŠ ą╗ąĖą│ą░ąĮą┤ą░ ą╝ąŠąČąĄčé čüą╗čāąČąĖčéčī ąŁąöąóąÉ (čŹčéąĖą╗ąĄąĮą┤ąĖą░ą╝ąĖąĮč鹥čéčĆą░čåąĄčéą░čé). ąØąĄąŠą▒čģąŠą┤ąĖą╝ąŠ ąĖą╝ąĄčéčī ą▓ ą▓ąĖą┤čā, čćč鹊 ą║ąŠą╗ąĖč湥čüčéą▓ąŠ ą┤ąŠąĮąŠčĆąĮčŗčģ čåąĄąĮčéčĆąŠą▓ ąĖ ą┤ąĄąĮčéą░čéąĮąŠčüčéčī ąĮąĄ ą▓čüąĄą│ą┤ą░ čüąŠą▓ą┐ą░ą┤ą░čÄčé.

ąÜą╗ą░čüčüąĖčäąĖą║ą░čåąĖčÅ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗčģ čüąŠąĄą┤ąĖąĮąĄąĮąĖą╣.
ą¤ąŠ ąĘą░čĆčÅą┤čā ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ ąĖąŠąĮą░:
ą░) ą║ą░čéąĖąŠąĮąĮčŗąĄ: 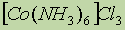 - ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
- ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
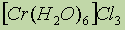 - ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 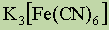 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
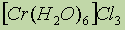 - ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 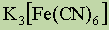 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 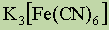 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).ą▓) ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
) ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ: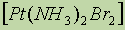 - ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
ą¤ąŠ ą┐čĆąĖčĆąŠą┤ąĄ ą╗ąĖą│ą░ąĮą┤ą░:
ą░) čü ąĮąĄą╣čéčĆą░ą╗čīąĮčŗą╝ąĖ ą╗ąĖą│ą░ąĮą┤ą░ą╝ąĖ: 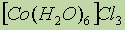 - ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
- ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.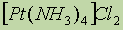 - č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
- č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.

ąÜą╗ą░čüčüąĖčäąĖą║ą░čåąĖčÅ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗčģ čüąŠąĄą┤ąĖąĮąĄąĮąĖą╣.
ą¤ąŠ ąĘą░čĆčÅą┤čā ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ ąĖąŠąĮą░:
ą░) ą║ą░čéąĖąŠąĮąĮčŗąĄ: 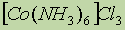 - ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
- ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
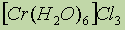 - ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 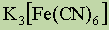 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
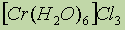 - ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 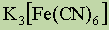 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ: 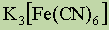 - ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III). - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).ą▓) ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
) ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ: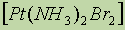 - ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
ą¤ąŠ ą┐čĆąĖčĆąŠą┤ąĄ ą╗ąĖą│ą░ąĮą┤ą░:
ą░) čü ąĮąĄą╣čéčĆą░ą╗čīąĮčŗą╝ąĖ ą╗ąĖą│ą░ąĮą┤ą░ą╝ąĖ: 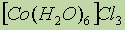 - ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
- ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.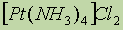 - č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
- č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
ąÜą╗ą░čüčüąĖčäąĖą║ą░čåąĖčÅ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗčģ čüąŠąĄą┤ąĖąĮąĄąĮąĖą╣.
ą¤ąŠ ąĘą░čĆčÅą┤čā ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ ąĖąŠąĮą░:ą░) ą║ą░čéąĖąŠąĮąĮčŗąĄ:
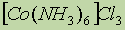
- ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
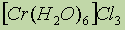
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
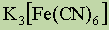
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
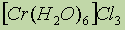
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
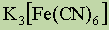
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
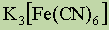
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).ą▓)
ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
)
ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
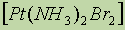
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
ą¤ąŠ ą┐čĆąĖčĆąŠą┤ąĄ ą╗ąĖą│ą░ąĮą┤ą░:ą░) čü ąĮąĄą╣čéčĆą░ą╗čīąĮčŗą╝ąĖ ą╗ąĖą│ą░ąĮą┤ą░ą╝ąĖ:
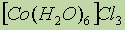
- ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
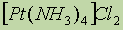
- č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
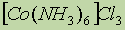
- ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
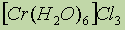
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
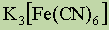
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
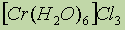
- ą│ąĄą║čüą░ą░ą║ą▓ą░čģčĆąŠą╝ą░ (III) čģą╗ąŠčĆąĖą┤. ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
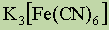
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą▒) ą░ąĮąĖąŠąĮąĮčŗąĄ:
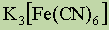
- ą║ą░ą╗ąĖčÅ ą│ąĄą║čüą░čåąĖą░ąĮąŠč乥čĆčĆą░čé (III).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
 - ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
- ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).
ą║ąŠą▒ą░ą╗čīčéą░ č鹥čéčĆą░čģą╗ąŠčĆą║ąŠą▒ą░ą╗čīčéą░čé (II).ą▓)
ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
)
ąĮąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
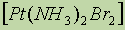
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
- ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).
ą¤ąŠ ą┐čĆąĖčĆąŠą┤ąĄ ą╗ąĖą│ą░ąĮą┤ą░:ą░) čü ąĮąĄą╣čéčĆą░ą╗čīąĮčŗą╝ąĖ ą╗ąĖą│ą░ąĮą┤ą░ą╝ąĖ:
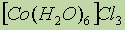
- ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
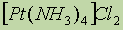
- č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
ą░) čü ąĮąĄą╣čéčĆą░ą╗čīąĮčŗą╝ąĖ ą╗ąĖą│ą░ąĮą┤ą░ą╝ąĖ:
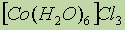
- ą│ąĄą║čüą░ą░ą║ą▓ą░ą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
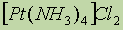
- č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
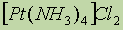
- č鹥čéčĆą░ą░ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮčŗ (III) čģą╗ąŠčĆąĖą┤.
ą▒) ą░čåąĖą┤ąŠą║ąŠą╝ą┐ą╗ąĄą║čüčŗ:
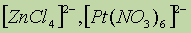
- č鹥čéčĆą░- ąĖ, čüąŠąŠčéą▓ąĄčéčüčéą▓ąĄąĮąĮąŠ, ą│ąĄą║čüą░-.ą▓) ą│ąĄč鹥čĆąŠą╗ąĖą│ą░ąĮą┤ąĮčŗąĄ:
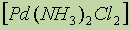
- ą┤ąĖčģą╗ąŠčĆą┤ąĖą░ą╝ą╝ąĖąĮą┐ą░ą╗ą╗ą░ą┤ąĖą╣ (II).
ąØąŠą╝ąĄąĮą║ą╗ą░čéčāčĆą░ (IUPAC).
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).
ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).
ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.
ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
IUPAC).
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).
ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).
ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.
ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
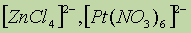
- č鹥čéčĆą░- ąĖ, čüąŠąŠčéą▓ąĄčéčüčéą▓ąĄąĮąĮąŠ, ą│ąĄą║čüą░-.ą▓) ą│ąĄč鹥čĆąŠą╗ąĖą│ą░ąĮą┤ąĮčŗąĄ:
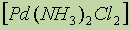
- ą┤ąĖčģą╗ąŠčĆą┤ąĖą░ą╝ą╝ąĖąĮą┐ą░ą╗ą╗ą░ą┤ąĖą╣ (II).
ąØąŠą╝ąĄąĮą║ą╗ą░čéčāčĆą░ (IUPAC).
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).
ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).
ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.
ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
IUPAC).
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).
ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).
ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.
ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
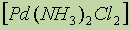
- ą┤ąĖčģą╗ąŠčĆą┤ąĖą░ą╝ą╝ąĖąĮą┐ą░ą╗ą╗ą░ą┤ąĖą╣ (II).
ąØąŠą╝ąĄąĮą║ą╗ą░čéčāčĆą░ (IUPAC).
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).
ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).
ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.
ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
IUPAC).
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).
ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).
ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.
ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
ąØąŠą╝ąĄąĮą║ą╗ą░čéčāčĆą░ (IUPAC).
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
IUPAC).
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
ąöą░ąĄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą║ą░čéąĖąŠąĮą░ (ą┐čĆąŠčüč鹊ą│ąŠ ąĖą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ).ąĢčüą╗ąĖ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ąĮąĄčŹą╗ąĄą║čéčĆąŠą╗ąĖčéąĮąŠą│ąŠ čéąĖą┐ą░ (ąĮąĄ ą┐ąŠą┤čĆą░ąĘą┤ąĄą╗čÅąĄčéčüčÅ ąĮą░ ą▓ąĮąĄčłąĮčÄčÄ ąĖ ą▓ąĮčāčéčĆąĄąĮąĮčÄčÄ čüč乥čĆčŗ), č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.ąĪč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čåąĄąĮčéčĆą░ą╗čīąĮąŠą│ąŠ ą░č鹊ą╝ą░ čāą║ą░ąĘčŗą▓ą░ąĄčéčüčÅ čĆąĖą╝čüą║ąĖą╝ąĖ čåąĖčäčĆą░ą╝ąĖ ą▓ ( ).ąØąĄą╣čéčĆą░ą╗čīąĮčŗąĄ ą╗ąĖą│ą░ąĮą┤čŗ ąĖą╝ąĄčÄčé č鹊 ąČąĄ ąĮą░ąĘą▓ą░ąĮąĖąĄ, čćč鹊 ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░.ąÜ ą╗ąĖą│ą░ąĮą┤ą░ą╝ ą░ąĮąĖąŠąĮą░ą╝ ąĮą░ ą║ąŠąĮčåąĄ ą┤ąŠą▒ą░ą▓ą╗čÅąĄčéčüčÅ ŌĆōąŠ.(NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).
ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.
ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.
ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
NH3 ŌĆō ą┤ą▓ą░ ŌĆōą╝ą╝- ą▓ ą║ąŠčĆąĮąĄ, ąŠčüčéą░ą╗čīąĮčŗąĄ ą┐čĆąŠąĖąĘą▓ąŠą┤ąĮčŗąĄ ŌĆō ąŠą┤ąĮąŠ ŌĆōą╝-).
ąöą╗čÅ čāą║ą░ąĘą░ąĮąĖčÅ ą║ąŠą╗ąĖč湥čüčéą▓ą░ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆąŠą▓ą░ąĮąĮčŗčģ ą╗ąĖą│ą░ąĮą┤ąŠą▓ ąĖčüą┐ąŠą╗čīąĘčāčÄčé ą│čĆąĄč湥čüą║ąĖąĄ ą┐čĆąĖčüčéą░ą▓ą║ąĖ (ą┤ąĖ-, čéčĆąĖ-, č鹥čéčĆą░- ąĖ.čé. ą┤.).ąØą░ąĘą▓ą░ąĮąĖąĄ ą║ąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą┐ąĖčłąĄčéčüčÅ ą▓ ąŠą┤ąĮąŠ čüą╗ąŠą▓ąŠ.ąÆ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ ąĖąŠąĮąĄ čüąĮą░čćą░ą╗ą░ čāą║ą░ąĘčŗą▓ą░čÄčéčüčÅ ąĮą░ąĘą▓ą░ąĮąĖčÅ ąĖąŠąĮąŠą▓, ą░ ą┐ąŠč鹊ą╝ ąĮąĄą╣čéčĆą░ą╗čīąĮčŗčģ ą╝ąŠą╗ąĄą║čāą╗.ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮčŗą╣ ąĖąŠąĮ ąĖą╝ąĄąĄčé ąŠčéčĆąĖčåą░č鹥ą╗čīąĮčŗą╣ ąĘą░čĆčÅą┤, č鹊 ąĄą│ąŠ ąĮą░ąĘą▓ą░ąĮąĖąĄ ąĘą░ą║ą░ąĮčćąĖą▓ą░ąĄčéčüčÅ ąĮą░ -ą░čé.
.
ą¤čĆąĖą╝ąĄčĆčŗ:
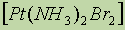
-
ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).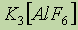 - ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆąŠą░ą╗čÄą╝ąĖąĮą░čé.
- ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆąŠą░ą╗čÄą╝ąĖąĮą░čé.
ą▒čĆąŠą╝
ą┤ąĖą░
ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░
(II).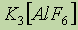 - ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆąŠą░ą╗čÄą╝ąĖąĮą░čé.
- ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆąŠą░ą╗čÄą╝ąĖąĮą░čé.
ą┤ąĖą▒čĆąŠą╝ą┤ąĖą░ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░ (II).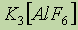 - ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆąŠą░ą╗čÄą╝ąĖąĮą░čé.
- ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆąŠą░ą╗čÄą╝ąĖąĮą░čé.
ą▒čĆąŠą╝
ą┤ąĖą░
ą╝ą╝ąĖąĮą┐ą╗ą░čéąĖąĮą░
(II).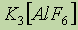 - ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆąŠą░ą╗čÄą╝ąĖąĮą░čé.
- ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆąŠą░ą╗čÄą╝ąĖąĮą░čé.
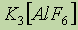
- ą║ą░ą╗ąĖą╣ ą│ąĄą║čüą░čäč鹊čĆ
ąŠą░ą╗čÄą╝ąĖąĮ
ą░čé.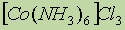
-
ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.ą░
ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
ą│ąĄą║čüą░ą░ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.ą░
ą╝ą╝ąĖąĮąŠą║ąŠą▒ą░ą╗čīčéą░ (III) čģą╗ąŠčĆąĖą┤.
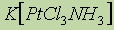
- ą║ą░ą╗ąĖčÅ
čéčĆąĖčģą╗ąŠčĆą░
ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮ
ą░čé (II).
ą║ą░ą╗ąĖčÅ
čéčĆąĖčģą╗ąŠčĆą░
ą╝ą╝ąĖąĮąŠą┐ą╗ą░čéąĖąĮ
ą░čé (II).
ąÜąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮąŠąĄ čćąĖčüą╗ąŠ. ąÜąŠąŠčĆą┤ąĖąĮą░čåąĖąŠąĮąĮčŗą╝ čćąĖčüą╗ąŠą╝ (ą║. čć.)ŌĆō ąŠą▒čŗčćąĮąŠ ąĮą░ąĘčŗą▓ą░čÄčé č鹊 ą║ąŠą╗ąĖč湥čüčéą▓ąŠ ą╗ąĖą│ą░ąĮą┤ąŠą▓, ą║ąŠč鹊čĆąŠąĄ čåąĄąĮčéčĆą░ą╗čīąĮčŗą╣ ą░č鹊ą╝ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆčāąĄčé ą▓ ą┤ąĄąĮąĮąŠą╝ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĖ.ąóą░ą║, ąĮą░ą┐čĆąĖą╝ąĄčĆ ą▓ ą▓čŗčłąĄą┐čĆąĖą▓ąĄą┤ąĄąĮąĮčŗčģ ą┐čĆąĖą╝ąĄčĆą░čģ ą║. čć. čüąŠąŠčéą▓ąĄčéčüčéą▓ąĄąĮąĮąŠ čĆą░ą▓ąĮčŗ: ą┐ą╗ą░čéąĖąĮą░ (II) ŌĆō 4, ą░ą╗čÄą╝ąĖąĮąĖą╣ ŌĆō 6, ą║ąŠą▒ą░ą╗čīčé ŌĆō 6, ą┐ą╗ą░čéąĖąĮą░ (II) ŌĆō 4.
(ą║. čć.)ŌĆō ąŠą▒čŗčćąĮąŠ ąĮą░ąĘčŗą▓ą░čÄčé č鹊 ą║ąŠą╗ąĖč湥čüčéą▓ąŠ ą╗ąĖą│ą░ąĮą┤ąŠą▓, ą║ąŠč鹊čĆąŠąĄ čåąĄąĮčéčĆą░ą╗čīąĮčŗą╣ ą░č鹊ą╝ ą║ąŠąŠčĆą┤ąĖąĮąĖčĆčāąĄčé ą▓ ą┤ąĄąĮąĮąŠą╝ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą╝ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĖ.ąóą░ą║, ąĮą░ą┐čĆąĖą╝ąĄčĆ ą▓ ą▓čŗčłąĄą┐čĆąĖą▓ąĄą┤ąĄąĮąĮčŗčģ ą┐čĆąĖą╝ąĄčĆą░čģ ą║. čć. čüąŠąŠčéą▓ąĄčéčüčéą▓ąĄąĮąĮąŠ čĆą░ą▓ąĮčŗ: ą┐ą╗ą░čéąĖąĮą░ (II) ŌĆō 4, ą░ą╗čÄą╝ąĖąĮąĖą╣ ŌĆō 6, ą║ąŠą▒ą░ą╗čīčé ŌĆō 6, ą┐ą╗ą░čéąĖąĮą░ (II) ŌĆō 4.
ąóą░ą║, ąĮą░ą┐čĆąĖą╝ąĄčĆ ą▓ ą▓čŗčłąĄą┐čĆąĖą▓ąĄą┤ąĄąĮąĮčŗčģ ą┐čĆąĖą╝ąĄčĆą░čģ ą║. čć. čüąŠąŠčéą▓ąĄčéčüčéą▓ąĄąĮąĮąŠ čĆą░ą▓ąĮčŗ: ą┐ą╗ą░čéąĖąĮą░ (II) ŌĆō 4, ą░ą╗čÄą╝ąĖąĮąĖą╣ ŌĆō 6, ą║ąŠą▒ą░ą╗čīčé ŌĆō 6, ą┐ą╗ą░čéąĖąĮą░ (II) ŌĆō 4.
ąÜąŠąĮčüčéą░ąĮčéą░ čāčüč鹊ą╣čćąĖą▓ąŠčüčéąĖ (ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÅ) ą║ąŠą╝ą┐ą╗ąĄą║čüąŠą▓. ąĢčüą╗ąĖ ą┐čĆąĄą┤čüčéą░ą▓ąĖčéčī čüčģąĄą╝ą░čéąĖčćąĮąŠ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ čĆąĄą░ą║čåąĖąĄą╣
ąĢčüą╗ąĖ ą┐čĆąĄą┤čüčéą░ą▓ąĖčéčī čüčģąĄą╝ą░čéąĖčćąĮąŠ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ čĆąĄą░ą║čåąĖąĄą╣
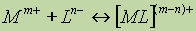
, č鹊ą║ąŠąĮčüčéą░ąĮčéą░ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÅ (čāčüč鹊ą╣čćąĖą▓ąŠčüčéąĖ) ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ąĘą░ą┐ąĖčłąĄčéčüčÅ čüą╗ąĄą┤čāčÄčēąĖą╝ ąŠą▒čĆą░ąĘąŠą╝:
, č鹊ą║ąŠąĮčüčéą░ąĮčéą░ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÅ (čāčüč鹊ą╣čćąĖą▓ąŠčüčéąĖ) ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ąĘą░ą┐ąĖčłąĄčéčüčÅ čüą╗ąĄą┤čāčÄčēąĖą╝ ąŠą▒čĆą░ąĘąŠą╝:
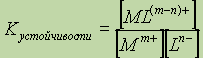
, ą│ą┤ąĄ
, ą│ą┤ąĄ[Mm+] ąĖ [Ln-] ą║ąŠąĮčåąĄąĮčéą░čåąĖąĖ ą╝ąĄčéą░ą╗ą╗ą░ ąĖ ą╗ąĖą│ą░ąĮą┤ą░ čüąŠąŠčéą▓ąĄčéčüčéą▓ąĄąĮąĮąŠ, ą░ [ML(m-n)+]- ]- ą║ąŠąĮčåąĄąĮčéčĆą░čåąĖčÅ ąŠą▒čĆą░ąĘčāčÄčēąĄą│ąŠčüčÅ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ. ąÜąŠąĮčüčéą░ąĮčéą░ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÅ ŌĆō ą▓ąĄą╗ąĖčćąĖąĮą░ ą▓čüąĄą│ą┤ą░ ą┐ąŠą╗ąŠąČąĖč鹥ą╗čīąĮą░čÅ.ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąŠąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄ ą┐čĆąŠč鹥ą║ą░ąĄčé čüčéčāą┐ąĄąĮčćą░č鹊, ą║ą░ą║, ąĮą░ą┐čĆąĖą╝ąĄčĆ, ą▓ čüą╗čāčćą░ąĄ:
ąĖ [Ln-] ą║ąŠąĮčåąĄąĮčéą░čåąĖąĖ ą╝ąĄčéą░ą╗ą╗ą░ ąĖ ą╗ąĖą│ą░ąĮą┤ą░ čüąŠąŠčéą▓ąĄčéčüčéą▓ąĄąĮąĮąŠ, ą░ [ML(m-n)+]- ]- ą║ąŠąĮčåąĄąĮčéčĆą░čåąĖčÅ ąŠą▒čĆą░ąĘčāčÄčēąĄą│ąŠčüčÅ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ. ąÜąŠąĮčüčéą░ąĮčéą░ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÅ ŌĆō ą▓ąĄą╗ąĖčćąĖąĮą░ ą▓čüąĄą│ą┤ą░ ą┐ąŠą╗ąŠąČąĖč鹥ą╗čīąĮą░čÅ.ąĢčüą╗ąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąŠąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄ ą┐čĆąŠč鹥ą║ą░ąĄčé čüčéčāą┐ąĄąĮčćą░č鹊, ą║ą░ą║, ąĮą░ą┐čĆąĖą╝ąĄčĆ, ą▓ čüą╗čāčćą░ąĄ:
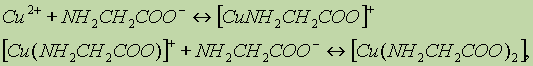
č鹊 ą┤ą╗čÅ ą║ą░ąČą┤ąŠą╣ čüčéą░ą┤ąĖąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąŠąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÅ ąĘą░ą┐ąĖčüčŗą▓ą░ąĄčéčüčÅ čüą▓ąŠčÅ čüčéčāą┐ąĄąĮčćą░čéą░čÅ ą║ąŠąĮčüčéą░ąĮčéą░ čāčüč鹊ą╣čćąĖą▓ąŠčüčéąĖ:
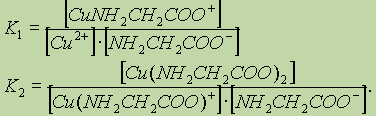
ą×ą▒čēą░čÅ ą║ąŠąĮčüčéą░ąĮčéą░ čāčüč鹊ą╣čćąĖą▓ąŠčüčéąĖ:
b = ąÜ1× ąÜ2.
ąÆą▓ąĖą┤čā č鹊ą│ąŠ, čćč鹊 ą║ąŠąĮčüčéą░ąĮčéčŗ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÅ ŌĆō ą▓ąĄą╗ąĖčćąĖąĮčŗ, ą║ą░ą║ ą┐čĆą░ą▓ąĖą╗ąŠ, ą╝ą░ą╗čŗąĄ, čāą┤ąŠą▒ąĮąŠ ą┐ąŠą╗čīąĘąŠą▓ą░čéčīčüčÅ ą╗ąŠą│ą░čĆąĖčäą╝ą░ą╝ąĖ ą║ąŠąĮčüčéą░ąĮčé:
log b = log ąÜ1 + log ąÜ2.
ą¤ąŠ č鹥ą╝ ąČąĄ ą┐čĆąĖčćąĖąĮą░ą╝ čćą░čēąĄ ą┐ąŠą╗čīąĘčāčÄčéčüčÅ
ą║ąŠąĮčüčéą░ąĮč鹊ą╣ ąĮąĄčüč鹊ą╣ą║ąŠčüčéąĖ ą║ąŠą╝ą┐ą╗ąĄą║čüąĮąŠą│ąŠ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ:
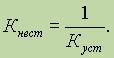
ąÜąŠąĮčüčéą░ąĮčéą░ ąĮąĄčüč鹊ą╣ą║ąŠčüčéąĖ ŌĆō ą▓ąĄą╗ąĖčćąĖąĮą░ ąŠčéčĆąĖčåą░č鹥ą╗čīąĮą░čÅ, čüą╗ąĄą┤ąŠą▓ą░č鹥ą╗čīąĮąŠ, č湥ą╝ ą╝ąĄąĮčīčłąĄ
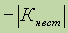
, č鹥ą╝ čāč鹊ą╣čćąĖą▓ąĄąĄ ą║ąŠą╝ą┐ą╗ąĄą║čü.ąĄ ą║ąŠą╝ą┐ą╗ąĄą║čü.
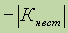
, č鹥ą╝ čāč鹊ą╣čćąĖą▓ąĄąĄ ą║ąŠą╝ą┐ą╗ąĄą║čü.


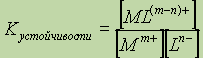 , ą│ą┤ąĄ
, ą│ą┤ąĄ