 |
 |
| ├ļÓŌĒÓ | ęÕ±“¹ ┼├▌ | ╩ĒĶŃĶ | ąÕ±¾±¹ | ┬Õß-ĻÓ“ÓļŅŃ | įŅ¾ņ | ╬ ’Ņ“ÓļÕ |
±ÕŃŅõĒ : ’ “ĒĶ÷Ó, 3 ņÓ 2024
|
||||||||||||
±ÕŃŅõĒ : ’ “ĒĶ÷Ó, 3 ņÓ 2024
|
||||||||||||
|
▌ļÕĻ“ŅĒĒÓ ßĶßļĶŅ“ÕĻÓ
ąÆąŠą┤ąŠčĆąŠą┤
ąØąĢą×ąĀąōąÉąØąśą¦ąĢąĪąÜąÉą» ąźąśą£ąśą». ąŁąøąĢą£ąĢąØąóą½ ąś ąśąź ąĪą×ąĢąöąśąØąĢąØąśą»1. ąÆąŠą┤ąŠčĆąŠą┤ąĪą▓ąŠą╣čüčéą▓ą░ 1H.
ąÉč鹊ą╝ ą▓ąŠą┤ąŠčĆąŠą┤ą░ čüąŠčüč鹊ąĖčé ąĖąĘ ąŠą┤ąĮąŠą│ąŠ ą┐čĆąŠč鹊ąĮą░ ąĖ ąŠą┤ąĮąŠą│ąŠ 菹╗ąĄą║čéčĆąŠąĮą░. ąŁč鹊čé ą┐čĆąŠčüč鹥ą╣čłąĖą╣ ą░č鹊ą╝ ąĮąĄ ąĖą╝ąĄąĄčé ą░ąĮą░ą╗ąŠą│ąŠą▓ ą▓ ą┐ąĄčĆąĖąŠą┤ąĖč湥čüą║ąŠą╣ čüąĖčüč鹥ą╝ąĄ. ą×ąĮ čüą┐ąŠčüąŠą▒ąĄąĮ č鹥čĆčÅčéčī 菹╗ąĄą║čéčĆąŠąĮ, ą┐čĆąĄą▓čĆą░čēą░čÅčüčī ą▓ ą║ą░čéąĖąŠąĮ ąØ+, ąĖ ą▓ čŹč鹊ą╝ ąŠčéąĮąŠčłąĄąĮąĖąĖ čüčģąŠą┤ąĄąĮ čüąŠ čēąĄą╗ąŠčćąĮčŗą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ, ą║ąŠč鹊čĆčŗąĄ čéą░ą║ąČąĄ ą┐čĆąŠčÅą▓ą╗čÅčÄčé čüč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ 1+. ąÉč鹊ą╝ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ą╝ąŠąČąĄčé čéą░ą║ąČąĄ ą┐čĆąĖčüąŠąĄą┤ąĖąĮčÅčéčī 菹╗ąĄą║čéčĆąŠąĮ, ąŠą▒čĆą░ąĘčāčÅ ą┐čĆąĖ čŹč鹊ą╝ ą░ąĮąĖąŠąĮ ąØ- , 菹╗ąĄą║čéčĆąŠąĮąĮą░čÅ ą║ąŠąĮčäąĖą│čāčĆą░čåąĖčÅ ą║ąŠč鹊čĆąŠą│ąŠ čéą░ą║ą░čÅ ąČąĄ, ą║ą░ą║ čā ą░č鹊ą╝ą░ ą│ąĄą╗ąĖčÅ. ąÆ čŹč鹊ą╝ ąŠčéąĮąŠčłąĄąĮąĖąĖ ą▓ąŠą┤ąŠčĆąŠą┤ čüčģąŠą┤ąĄąĮ čü ą│ą░ą╗ąŠą│ąĄąĮą░ą╝ąĖ, ą░ąĮąĖąŠąĮčŗ ą║ąŠč鹊čĆčŗčģ ąĖą╝ąĄčÄčé 菹╗ąĄą║čéčĆąŠąĮąĮčŗąĄ ą║ąŠąĮčäąĖą│čāčĆą░čåąĖąĖ čüąŠčüąĄą┤ąĮąĖčģ ą▒ą╗ą░ą│ąŠčĆąŠą┤ąĮčŗčģ ą│ą░ąĘąŠą▓.ąóą░ą║ąĖą╝ ąŠą▒čĆą░ąĘąŠą╝, ą▓ąŠą┤ąŠčĆąŠą┤ ąĖą╝ąĄąĄčé ą┤ą▓ąŠą╣čüčéą▓ąĄąĮąĮčāčÄ ą┐čĆąĖčĆąŠą┤čā, ą┐čĆąŠčÅą▓ą╗čÅčÅ ą║ą░ą║ ąŠą║ąĖčüą╗ąĖč鹥ą╗čīąĮčāčÄ, čéą░ą║ ąĖ ą▓ąŠčüčüčéą░ąĮąŠą▓ąĖč鹥ą╗čīąĮčāčÄ čüą┐ąŠčüąŠą▒ąĮąŠčüčéčī. ą¤ąŠ čŹč鹊ą╣ ą┐čĆąĖčćąĖąĮąĄ ą▓ ąŠą┤ąĮąĖčģ čüą╗čāčćą░čÅčģ ą▓ąŠą┤ąŠčĆąŠą┤ ą┐ąŠą╝ąĄčēą░čÄčé ą▓ ą┐ąŠą┤ą│čĆčāą┐ą┐čā čēąĄą╗ąŠčćąĮčŗčģ ą╝ąĄčéą░ą╗ą╗ąŠą▓, ą▓ ą┤čĆčāą│ąĖčģ ŌĆö ą▓ ą┐ąŠą┤ą│čĆčāą┐ą┐čā ą│ą░ą╗ąŠą│ąĄąĮąŠą▓. ąźąĖą╝ąĖč湥čüą║ąĖąĄ čüą▓ąŠą╣čüčéą▓ą░. ąŁąĮąĄčĆą│ąĖčÅ čüą▓čÅąĘąĖ ą▓ ą╝ąŠą╗ąĄą║čāą╗ąĄ ą▓ąŠą┤ąŠčĆąŠą┤ą░ H2 čüąŠčüčéą░ą▓ą╗čÅąĄčé 436 ą║ąöąČ/ą╝ąŠą╗čī. ąæąŠą╗čīčłą░čÅ ą▓ąĄą╗ąĖčćąĖąĮą░ 菹ĮąĄčĆą│ąĖąĖ čüą▓čÅąĘąĖ ąŠą▒čŖčÅčüąĮčÅąĄčé čüčĆą░ą▓ąĮąĖč鹥ą╗čīąĮąŠ ą╝ą░ą╗čāčÄ ą░ą║čéąĖą▓ąĮąŠčüčéčī ą╝ąŠą╗ąĄą║čāą╗čÅčĆąĮąŠą│ąŠ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ą┐čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ. ąóą░ą║, ą┐čĆąĖ ą║ąŠą╝ąĮą░čéąĮąŠą╣ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĄ ą▓ąŠą┤ąŠčĆąŠą┤ čĆąĄą░ą│ąĖčĆčāąĄčé ą╗ąĖčłčī čü čäč鹊čĆąŠą╝: ąŁąĮąĄčĆą│ąĖčÅ čüą▓čÅąĘąĖ ą▓ ą╝ąŠą╗ąĄą║čāą╗ąĄ ą▓ąŠą┤ąŠčĆąŠą┤ą░ +, ąĖ ą▓ čŹč鹊ą╝ ąŠčéąĮąŠčłąĄąĮąĖąĖ čüčģąŠą┤ąĄąĮ čüąŠ čēąĄą╗ąŠčćąĮčŗą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ, ą║ąŠč鹊čĆčŗąĄ čéą░ą║ąČąĄ ą┐čĆąŠčÅą▓ą╗čÅčÄčé čüč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ 1+. ąÉč鹊ą╝ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ą╝ąŠąČąĄčé čéą░ą║ąČąĄ ą┐čĆąĖčüąŠąĄą┤ąĖąĮčÅčéčī 菹╗ąĄą║čéčĆąŠąĮ, ąŠą▒čĆą░ąĘčāčÅ ą┐čĆąĖ čŹč鹊ą╝ ą░ąĮąĖąŠąĮ ąØ- , 菹╗ąĄą║čéčĆąŠąĮąĮą░čÅ ą║ąŠąĮčäąĖą│čāčĆą░čåąĖčÅ ą║ąŠč鹊čĆąŠą│ąŠ čéą░ą║ą░čÅ ąČąĄ, ą║ą░ą║ čā ą░č鹊ą╝ą░ ą│ąĄą╗ąĖčÅ. ąÆ čŹč鹊ą╝ ąŠčéąĮąŠčłąĄąĮąĖąĖ ą▓ąŠą┤ąŠčĆąŠą┤ čüčģąŠą┤ąĄąĮ čü ą│ą░ą╗ąŠą│ąĄąĮą░ą╝ąĖ, ą░ąĮąĖąŠąĮčŗ ą║ąŠč鹊čĆčŗčģ ąĖą╝ąĄčÄčé 菹╗ąĄą║čéčĆąŠąĮąĮčŗąĄ ą║ąŠąĮčäąĖą│čāčĆą░čåąĖąĖ čüąŠčüąĄą┤ąĮąĖčģ ą▒ą╗ą░ą│ąŠčĆąŠą┤ąĮčŗčģ ą│ą░ąĘąŠą▓.ąóą░ą║ąĖą╝ ąŠą▒čĆą░ąĘąŠą╝, ą▓ąŠą┤ąŠčĆąŠą┤ ąĖą╝ąĄąĄčé ą┤ą▓ąŠą╣čüčéą▓ąĄąĮąĮčāčÄ ą┐čĆąĖčĆąŠą┤čā, ą┐čĆąŠčÅą▓ą╗čÅčÅ ą║ą░ą║ ąŠą║ąĖčüą╗ąĖč鹥ą╗čīąĮčāčÄ, čéą░ą║ ąĖ ą▓ąŠčüčüčéą░ąĮąŠą▓ąĖč鹥ą╗čīąĮčāčÄ čüą┐ąŠčüąŠą▒ąĮąŠčüčéčī. ą¤ąŠ čŹč鹊ą╣ ą┐čĆąĖčćąĖąĮąĄ ą▓ ąŠą┤ąĮąĖčģ čüą╗čāčćą░čÅčģ ą▓ąŠą┤ąŠčĆąŠą┤ ą┐ąŠą╝ąĄčēą░čÄčé ą▓ ą┐ąŠą┤ą│čĆčāą┐ą┐čā čēąĄą╗ąŠčćąĮčŗčģ ą╝ąĄčéą░ą╗ą╗ąŠą▓, ą▓ ą┤čĆčāą│ąĖčģ ŌĆö ą▓ ą┐ąŠą┤ą│čĆčāą┐ą┐čā ą│ą░ą╗ąŠą│ąĄąĮąŠą▓. ąźąĖą╝ąĖč湥čüą║ąĖąĄ čüą▓ąŠą╣čüčéą▓ą░. ąŁąĮąĄčĆą│ąĖčÅ čüą▓čÅąĘąĖ ą▓ ą╝ąŠą╗ąĄą║čāą╗ąĄ ą▓ąŠą┤ąŠčĆąŠą┤ą░ H2 čüąŠčüčéą░ą▓ą╗čÅąĄčé 436 ą║ąöąČ/ą╝ąŠą╗čī. ąæąŠą╗čīčłą░čÅ ą▓ąĄą╗ąĖčćąĖąĮą░ 菹ĮąĄčĆą│ąĖąĖ čüą▓čÅąĘąĖ ąŠą▒čŖčÅčüąĮčÅąĄčé čüčĆą░ą▓ąĮąĖč鹥ą╗čīąĮąŠ ą╝ą░ą╗čāčÄ ą░ą║čéąĖą▓ąĮąŠčüčéčī ą╝ąŠą╗ąĄą║čāą╗čÅčĆąĮąŠą│ąŠ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ą┐čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ. ąóą░ą║, ą┐čĆąĖ ą║ąŠą╝ąĮą░čéąĮąŠą╣ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĄ ą▓ąŠą┤ąŠčĆąŠą┤ čĆąĄą░ą│ąĖčĆčāąĄčé ą╗ąĖčłčī čü čäč鹊čĆąŠą╝: ąŁąĮąĄčĆą│ąĖčÅ čüą▓čÅąĘąĖ ą▓ ą╝ąŠą╗ąĄą║čāą╗ąĄ ą▓ąŠą┤ąŠčĆąŠą┤ą░ H2 čüąŠčüčéą░ą▓ą╗čÅąĄčé 436 ą║ąöąČ/ą╝ąŠą╗čī. ąæąŠą╗čīčłą░čÅ ą▓ąĄą╗ąĖčćąĖąĮą░ 菹ĮąĄčĆą│ąĖąĖ čüą▓čÅąĘąĖ ąŠą▒čŖčÅčüąĮčÅąĄčé čüčĆą░ą▓ąĮąĖč鹥ą╗čīąĮąŠ ą╝ą░ą╗čāčÄ ą░ą║čéąĖą▓ąĮąŠčüčéčī ą╝ąŠą╗ąĄą║čāą╗čÅčĆąĮąŠą│ąŠ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ą┐čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ. ąóą░ą║, ą┐čĆąĖ ą║ąŠą╝ąĮą░čéąĮąŠą╣ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĄ ą▓ąŠą┤ąŠčĆąŠą┤ čĆąĄą░ą│ąĖčĆčāąĄčé ą╗ąĖčłčī čü čäč鹊čĆąŠą╝: ąĖ čü čģą╗ąŠčĆąŠą╝ ą┐čĆąĖ čāą╗čīčéčĆą░čäąĖąŠą╗ąĄč鹊ą▓ąŠą╝ ąŠą▒ą╗čāč湥ąĮąĖąĖ. ą¤čĆąĖ ą┐ąŠą▓čŗčłąĄąĮąĮąŠą╣ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĄ ą▓ąŠą┤ąŠčĆąŠą┤ čĆąĄą░ą│ąĖčĆčāąĄčé čüąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ą▓ąĄčēąĄčüčéą▓ą░ą╝ąĖ: ąŠąĮ čüą│ąŠčĆą░ąĄčé ą▓ ą░čéą╝ąŠčüč乥čĆąĄ ą║ąĖčüą╗ąŠčĆąŠą┤ą░ čü ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄą╝ ą▓ąŠą┤čŗ ąĖ ą▓čŗą┤ąĄą╗ąĄąĮąĖąĄą╝ ą▒ąŠą╗čīčłąŠą│ąŠ ą║ąŠą╗ąĖč湥čüčéą▓ą░ č鹥ą┐ą╗ąŠčéčŗ: ąĪąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą▓ąŠą┤ąŠčĆąŠą┤ą░ čü ąĮąĄą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ. ą¤čĆąĖ ąĮą░ą│čĆąĄą▓ą░ąĮąĖąĖ ą▓ąŠą┤ąŠčĆąŠą┤ ąŠą▒čĆą░čéąĖą╝ąŠ čĆąĄą░ą│ąĖčĆčāąĄčé čéą░ą║ąČąĄ čü ą▒čĆąŠą╝ąŠą╝, ąĖąŠą┤ąŠą╝, čüąĄčĆąŠą╣ ąĖ ą░ąĘąŠč鹊ą╝, ą┐čĆąĖč湥ą╝ čü ą┐ąŠčüą╗ąĄą┤ąĮąĖą╝ č鹊ą╗čīą║ąŠ ą▓ ą┐čĆąĖčüčāčéčüčéą▓ąĖąĖ ą║ą░čéą░ą╗ąĖąĘą░č鹊čĆą░ ąĖ ą┐čĆąĖ ą▓čŗčüąŠą║ąŠą╝ ą┤ą░ą▓ą╗ąĄąĮąĖąĖ. ąÆąŠą┤ąŠčĆąŠą┤ ą┐čĆąĖ ąĮą░ą│čĆąĄą▓ą░ąĮąĖąĖ čüą┐ąŠčüąŠą▒ąĄąĮ čĆąĄą░ą│ąĖčĆąŠą▓ą░čéčī ąĮąĄ č鹊ą╗čīą║ąŠ čü ą┐čĆąŠčüčéčŗą╝ąĖ, ąĮąŠ ąĖ čüąŠ čüą╗ąŠąČąĮčŗą╝ąĖ ą▓ąĄčēąĄčüčéą▓ą░ą╝ąĖ: ą¤čĆąĖ ąĮą░ą│čĆąĄą▓ą░ąĮąĖąĖ ą▓ąŠą┤ąŠčĆąŠą┤ ąŠą▒čĆą░čéąĖą╝ąŠ čĆąĄą░ą│ąĖčĆčāąĄčé čéą░ą║ąČąĄ čü ą▒čĆąŠą╝ąŠą╝, ąĖąŠą┤ąŠą╝, čüąĄčĆąŠą╣ ąĖ ą░ąĘąŠč鹊ą╝, ą┐čĆąĖč湥ą╝ čü ą┐ąŠčüą╗ąĄą┤ąĮąĖą╝ č鹊ą╗čīą║ąŠ ą▓ ą┐čĆąĖčüčāčéčüčéą▓ąĖąĖ ą║ą░čéą░ą╗ąĖąĘą░č鹊čĆą░ ąĖ ą┐čĆąĖ ą▓čŗčüąŠą║ąŠą╝ ą┤ą░ą▓ą╗ąĄąĮąĖąĖ. ąÆąŠą┤ąŠčĆąŠą┤ ą┐čĆąĖ ąĮą░ą│čĆąĄą▓ą░ąĮąĖąĖ čüą┐ąŠčüąŠą▒ąĄąĮ čĆąĄą░ą│ąĖčĆąŠą▓ą░čéčī ąĮąĄ č鹊ą╗čīą║ąŠ čü ą┐čĆąŠčüčéčŗą╝ąĖ, ąĮąŠ ąĖ čüąŠ čüą╗ąŠąČąĮčŗą╝ąĖ ą▓ąĄčēąĄčüčéą▓ą░ą╝ąĖ: 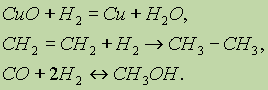 ąÆąŠ ą▓čüąĄčģ čĆą░čüčüą╝ą░čéčĆąĖą▓ą░ąĄą╝čŗčģ čĆąĄą░ą║čåąĖčÅčģ ą▓ąŠą┤ąŠčĆąŠą┤ čÅą▓ą╗čÅąĄčéčüčÅ ą▓ąŠčüčüčéą░ąĮąŠą▓ąĖč鹥ą╗ąĄą╝, ąŠą▒čĆą░ąĘčāčÅ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ, ą│ą┤ąĄ ąĄą│ąŠ čüč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čĆą░ą▓ąĮą░ 1+. ąĪąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą▓ąŠą┤ąŠčĆąŠą┤ą░ čü ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ. ąĪąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ ą▓ąŠą┤ąŠčĆąŠą┤ ą▓čüčéčāą┐ą░ąĄčé ą▓ čĆąĄą░ą║čåąĖąĖ ą┐čĆąĖ ą┐ąŠą▓čŗčłąĄąĮąĮčŗčģ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĄ ąĖ ą┤ą░ą▓ą╗ąĄąĮąĖąĖ čü ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄą╝ ą│ąĖą┤čĆąĖą┤ąŠą▓ (NaH, KH, ąĪą░ąØ2, ą│ą┤ąĄ ąĄą│ąŠ čüč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čĆą░ą▓ąĮą░ 1-: 1-: ąĪąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ ą▓ąŠą┤ąŠčĆąŠą┤ ą▓čüčéčāą┐ą░ąĄčé ą▓ čĆąĄą░ą║čåąĖąĖ ą┐čĆąĖ ą┐ąŠą▓čŗčłąĄąĮąĮčŗčģ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĄ ąĖ ą┤ą░ą▓ą╗ąĄąĮąĖąĖ čü ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄą╝ ą│ąĖą┤čĆąĖą┤ąŠą▓ (NaH, KH, ąĪą░ąØ2, ą│ą┤ąĄ ąĄą│ąŠ čüč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ čĆą░ą▓ąĮą░ 1-: 1-: ąōąĖą┤čĆąĖą┤ ąĮą░čéčĆąĖčÅ ŌĆö ą▒ąĄą╗ąŠąĄ ą║čĆąĖčüčéą░ą╗ą╗ąĖč湥čüą║ąŠąĄ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ, ą┐ąŠ čäąĖąĘąĖč湥čüą║ąĖą╝ čüą▓ąŠą╣čüčéą▓ą░ą╝ ąĮą░ą┐ąŠą╝ąĖąĮą░čÄčēąĄąĄ čģą╗ąŠčĆąĖą┤ ąĮą░čéčĆąĖčÅ. ą×ą┤ąĮą░ą║ąŠ čģąĖą╝ąĖč湥čüą║ąĖąĄ čüą▓ąŠą╣čüčéą▓ą░ NaH ąĖ NaCI čüąĖą╗čīąĮąŠ čĆą░ąĘą╗ąĖčćą░čÄčéčüčÅ. ąóą░ą║, čģą╗ąŠčĆąĖą┤ ąĮą░čéčĆąĖčÅ čĆą░čüčéą▓ąŠčĆčÅąĄčéčüčÅ ą▓ ą▓ąŠą┤ąĄ ąĖ ą┤ąĖčüčüąŠčåąĖąĖčĆčāąĄčé ą▓ čĆą░čüčéą▓ąŠčĆąĄ ąĮą░ ąĖąŠąĮčŗ. ąōąĖą┤čĆąĖą┤ ąĮą░čéčĆąĖčÅ ą▓ąŠą┤ąŠą╣ čĆą░ąĘą╗ą░ą│ą░ąĄčéčüčÅ čü ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄą╝ čēąĄą╗ąŠčćąĖ ąĖ ą▓ąŠą┤ąŠčĆąŠą┤ą░: NaCI čüąĖą╗čīąĮąŠ čĆą░ąĘą╗ąĖčćą░čÄčéčüčÅ. ąóą░ą║, čģą╗ąŠčĆąĖą┤ ąĮą░čéčĆąĖčÅ čĆą░čüčéą▓ąŠčĆčÅąĄčéčüčÅ ą▓ ą▓ąŠą┤ąĄ ąĖ ą┤ąĖčüčüąŠčåąĖąĖčĆčāąĄčé ą▓ čĆą░čüčéą▓ąŠčĆąĄ ąĮą░ ąĖąŠąĮčŗ. ąōąĖą┤čĆąĖą┤ ąĮą░čéčĆąĖčÅ ą▓ąŠą┤ąŠą╣ čĆą░ąĘą╗ą░ą│ą░ąĄčéčüčÅ čü ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖąĄą╝ čēąĄą╗ąŠčćąĖ ąĖ ą▓ąŠą┤ąŠčĆąŠą┤ą░: ą¤ąŠą╗čāč湥ąĮąĖąĄ. ąöą╗čÅ ą┐čĆąŠą╝čŗčłą╗ąĄąĮąĮąŠą│ąŠ ą┐ąŠą╗čāč湥ąĮąĖčÅ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ąĖčüą┐ąŠą╗čīąĘčāčÄčé čüą╗ąĄą┤čāčÄčēąĖąĄ čüą┐ąŠčüąŠą▒čŗ: 1. ąŁą╗ąĄą║čéčĆąŠą╗ąĖąĘ ą▓ąŠą┤ąĮčŗčģ čĆą░čüčéą▓ąŠčĆąŠą▓ čģą╗ąŠčĆąĖą┤ąŠą▓. 2. ą¤čĆąŠą┐čāčüą║ą░ąĮąĖąĄ ą┐ą░čĆąŠą▓ ą▓ąŠą┤čŗ ąĮą░ą┤ čĆą░čüą║ą░ą╗ąĄąĮąĮčŗą╝ čāą│ą╗ąĄą╝ ą┐čĆąĖ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĄ 1000 ┬░ąĪ: ąöą╗čÅ ą┐čĆąŠą╝čŗčłą╗ąĄąĮąĮąŠą│ąŠ ą┐ąŠą╗čāč湥ąĮąĖčÅ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ąĖčüą┐ąŠą╗čīąĘčāčÄčé čüą╗ąĄą┤čāčÄčēąĖąĄ čüą┐ąŠčüąŠą▒čŗ:1. ąŁą╗ąĄą║čéčĆąŠą╗ąĖąĘ ą▓ąŠą┤ąĮčŗčģ čĆą░čüčéą▓ąŠčĆąŠą▓ čģą╗ąŠčĆąĖą┤ąŠą▓. 2. ą¤čĆąŠą┐čāčüą║ą░ąĮąĖąĄ ą┐ą░čĆąŠą▓ ą▓ąŠą┤čŗ ąĮą░ą┤ čĆą░čüą║ą░ą╗ąĄąĮąĮčŗą╝ čāą│ą╗ąĄą╝ ą┐čĆąĖ č鹥ą╝ą┐ąĄčĆą░čéčāčĆąĄ 1000 ┬░ąĪ: 3. ąÜąŠąĮą▓ąĄčĆčüąĖčÅ ą╝ąĄčéą░ąĮą░ ą┐čĆąĖ ą▓čŗčüąŠą║ąĖčģ č鹥ą╝ą┐ąĄčĆą░čéčāčĆą░čģ: 4. ąÜčĆąĄą║ąĖąĮą│ čāą│ą╗ąĄą▓ąŠą┤ąŠčĆąŠą┤ąŠą▓. ąöą╗čÅ ą╗ą░ą▒ąŠčĆą░č鹊čĆąĮąŠą│ąŠ ą┐ąŠą╗čāč湥ąĮąĖčÅ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ąĖčüą┐ąŠą╗čīąĘčāčÄčé čüą╗ąĄą┤čāčÄčēąĖąĄ čüą┐ąŠčüąŠą▒čŗ: 1. ąÆąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĄ ą╝ąĄčéą░ą╗ą╗ąŠą▓ čü ą║ąĖčüą╗ąŠčéą░ą╝ąĖ: ąöą╗čÅ ą╗ą░ą▒ąŠčĆą░č鹊čĆąĮąŠą│ąŠ ą┐ąŠą╗čāč湥ąĮąĖčÅ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ąĖčüą┐ąŠą╗čīąĘčāčÄčé čüą╗ąĄą┤čāčÄčēąĖąĄ čüą┐ąŠčüąŠą▒čŗ: 1. ąÆąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĄ ą╝ąĄčéą░ą╗ą╗ąŠą▓ čü ą║ąĖčüą╗ąŠčéą░ą╝ąĖ: 2. ąÆąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĄ čēąĄą╗ąŠčćąĮąŠąĘąĄą╝ąĄą╗čīąĮčŗčģ ą╝ąĄčéą░ą╗ą╗ąŠą▓ čü ą▓ąŠą┤ąŠą╣: čü ą▓ąŠą┤ąŠą╣: 3. ąÆąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĄ ą░ą╗čÄą╝ąĖąĮąĖčÅ ąĖą╗ąĖ ą║čĆąĄą╝ąĮąĖčÅ čü ą▓ąŠą┤ąĮčŗą╝ąĖ čĆą░čüčéą▓ąŠčĆą░ą╝ąĖ čēąĄą╗ąŠč湥ą╣: 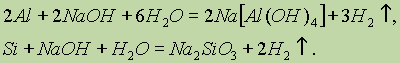 4. ąÆąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĄ ą│ąĖą┤čĆąĖą┤ąŠą▓ čü ą▓ąŠą┤ąŠą╣. ąÆąŠą┤ą░. ą×ą║čüąĖą┤ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ŌĆö ąŠą┤ąĮąŠ ąĖąĘ ąĮą░ąĖą▒ąŠą╗ąĄąĄ čĆą░čüą┐čĆąŠčüčéčĆą░ąĮąĄąĮąĮčŗčģ ąĖ ą▓ą░ąČąĮčŗčģ ą▓ąĄčēąĄčüčéą▓. ą¤ąŠą▓ąĄčĆčģąĮąŠčüčéčī ąŚąĄą╝ą╗ąĖ, ąĘą░ąĮčÅčéą░čÅ ą▓ąŠą┤ąŠą╣, ą▓ 2,5 čĆą░ąĘą░ ą▒ąŠą╗čīčłąĄ ą┐ąŠą▓ąĄčĆčģąĮąŠčüčéąĖ čüčāčłąĖ. ą¦ąĖčüč鹊ą╣ ą▓ąŠą┤čŗ ą▓ ą┐čĆąĖčĆąŠą┤ąĄ ąĮąĄčé, ŌĆö ąŠąĮą░ ą▓čüąĄą│ą┤ą░ čüąŠą┤ąĄčƹȹĖčé ą┐čĆąĖą╝ąĄčüąĖ. ą¤ąŠą╗čāčćą░čÄčé čćąĖčüčéčāčÄ ą▓ąŠą┤čā ą╝ąĄč鹊ą┤ąŠą╝ ą┐ąĄčĆąĄą│ąŠąĮą║ąĖ. ą¤ąĄčĆąĄą│ąĮą░ąĮąĮą░čÅ ą▓ąŠą┤ą░ ąĮą░ąĘčŗą▓ą░ąĄčéčüčÅ ą┤ąĖčüčéąĖą╗ą╗ąĖčĆąŠą▓ą░ąĮąĮąŠą╣. ąĪąŠčüčéą░ą▓ ą▓ąŠą┤čŗ (ą┐ąŠ ą╝ą░čüčüąĄ): 11,19 % ą▓ąŠą┤ąŠčĆąŠą┤ą░ ąĖ 88,81 % ą║ąĖčüą╗ąŠčĆąŠą┤ą░. ą×ą║čüąĖą┤ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ŌĆö ąŠą┤ąĮąŠ ąĖąĘ ąĮą░ąĖą▒ąŠą╗ąĄąĄ čĆą░čüą┐čĆąŠčüčéčĆą░ąĮąĄąĮąĮčŗčģ ąĖ ą▓ą░ąČąĮčŗčģ ą▓ąĄčēąĄčüčéą▓. ą¤ąŠą▓ąĄčĆčģąĮąŠčüčéčī ąŚąĄą╝ą╗ąĖ, ąĘą░ąĮčÅčéą░čÅ ą▓ąŠą┤ąŠą╣, ą▓ 2,5 čĆą░ąĘą░ ą▒ąŠą╗čīčłąĄ ą┐ąŠą▓ąĄčĆčģąĮąŠčüčéąĖ čüčāčłąĖ. ą¦ąĖčüč鹊ą╣ ą▓ąŠą┤čŗ ą▓ ą┐čĆąĖčĆąŠą┤ąĄ ąĮąĄčé, ŌĆö ąŠąĮą░ ą▓čüąĄą│ą┤ą░ čüąŠą┤ąĄčƹȹĖčé ą┐čĆąĖą╝ąĄčüąĖ. ą¤ąŠą╗čāčćą░čÄčé čćąĖčüčéčāčÄ ą▓ąŠą┤čā ą╝ąĄč鹊ą┤ąŠą╝ ą┐ąĄčĆąĄą│ąŠąĮą║ąĖ. ą¤ąĄčĆąĄą│ąĮą░ąĮąĮą░čÅ ą▓ąŠą┤ą░ ąĮą░ąĘčŗą▓ą░ąĄčéčüčÅ ą┤ąĖčüčéąĖą╗ą╗ąĖčĆąŠą▓ą░ąĮąĮąŠą╣. ąĪąŠčüčéą░ą▓ ą▓ąŠą┤čŗ (ą┐ąŠ ą╝ą░čüčüąĄ): 11,19 % ą▓ąŠą┤ąŠčĆąŠą┤ą░ ąĖ 88,81 % ą║ąĖčüą╗ąŠčĆąŠą┤ą░. 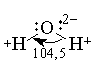 ążąĖąĘąĖč湥čüą║ąĖąĄ čüą▓ąŠą╣čüčéą▓ą░. ą¦ąĖčüčéą░čÅ ą▓ąŠą┤ą░ ą┐čĆąŠąĘčĆą░čćąĮą░, ąĮąĄ ąĖą╝ąĄąĄčé ąĘą░ą┐ą░čģą░ ąĖ ą▓ą║čāčüą░. ąØą░ąĖą▒ąŠą╗čīčłčāčÄ ą┐ą╗ąŠčéąĮąŠčüčéčī ąŠąĮą░ ąĖą╝ąĄąĄčé ą┐čĆąĖ 0 ┬░ąĪ (1 ą│/čüą╝ ą¦ąĖčüčéą░čÅ ą▓ąŠą┤ą░ ą┐čĆąŠąĘčĆą░čćąĮą░, ąĮąĄ ąĖą╝ąĄąĄčé ąĘą░ą┐ą░čģą░ ąĖ ą▓ą║čāčüą░. ąØą░ąĖą▒ąŠą╗čīčłčāčÄ ą┐ą╗ąŠčéąĮąŠčüčéčī ąŠąĮą░ ąĖą╝ąĄąĄčé ą┐čĆąĖ 0 ┬░ąĪ (1 ą│/čüą╝3). ą¤ą╗ąŠčéąĮąŠčüčéčī ą╗čīą┤ą░ ą╝ąĄąĮčīčłąĄ ą┐ą╗ąŠčéąĮąŠčüčéąĖ ąČąĖą┤ą║ąŠą╣ ą▓ąŠą┤čŗ, ą┐ąŠčŹč鹊ą╝čā ą╗ąĄą┤ ą▓čüą┐ą╗čŗą▓ą░ąĄčé ąĮą░ ą┐ąŠą▓ąĄčĆčģąĮąŠčüčéčī. ąÆąŠą┤ą░ ąĘą░ą╝ąĄčƹʹ░ąĄčé ą┐čĆąĖ 0 ┬░ąĪ ąĖ ą║ąĖą┐ąĖčé ą┐čĆąĖ 100┬░ ąĪ ą┐čĆąĖ ą┤ą░ą▓ą╗ąĄąĮąĖąĖ 101 325 ą¤ą░. ą×ąĮą░ ą┐ą╗ąŠčģąŠ ą┐čĆąŠą▓ąŠą┤ąĖčé č鹥ą┐ą╗ąŠčéčā ąĖ ąŠč湥ąĮčī ą┐ą╗ąŠčģąŠ ą┐čĆąŠą▓ąŠą┤ąĖčé 菹╗ąĄą║čéčĆąĖč湥čüčéą▓ąŠ. ąÆąŠą┤ą░ ŌĆö čģąŠčĆąŠčłąĖą╣ čĆą░čüčéą▓ąŠčĆąĖč鹥ą╗čī. ą£ąŠą╗ąĄą║čāą╗ą░ ą▓ąŠą┤čŗ ąĖą╝ąĄąĄčé čāą│ą╗ąŠą▓čāčÄ č乊čĆą╝čā: ą░č鹊ą╝čŗ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ą┐ąŠ ąŠčéąĮąŠčłąĄąĮąĖčÄ ą║ ą║ąĖčüą╗ąŠčĆąŠą┤čā ąŠą▒čĆą░ąĘčāčÄčé čāą│ąŠą╗, čĆą░ą▓ąĮčŗą╣ 104,5┬░. ą¤ąŠčŹč鹊ą╝čā ą╝ąŠą╗ąĄą║čāą╗ą░ ą▓ąŠą┤čŗ ŌĆö ą┤ąĖą┐ąŠą╗čī: čéą░ čćą░čüčéčī ą╝ąŠą╗ąĄą║čāą╗čŗ, ą│ą┤ąĄ ąĮą░čģąŠą┤ąĖčéčüčÅ ą▓ąŠą┤ąŠčĆąŠą┤, ąĘą░čĆčÅąČąĄąĮą░ ą┐ąŠą╗ąŠąČąĖč鹥ą╗čīąĮąŠ, ą░ čćą░čüčéčī, ą│ą┤ąĄ ąĮą░čģąŠą┤ąĖčéčüčÅ ą║ąĖčüą╗ąŠčĆąŠą┤, ŌĆö ąŠčéčĆąĖčåą░č鹥ą╗čīąĮąŠ. ąæą╗ą░ą│ąŠą┤ą░čĆčÅ ą┐ąŠą╗čÅčĆąĮąŠčüčéąĖ ą╝ąŠą╗ąĄą║čāą╗ ą▓ąŠą┤čŗ 菹╗ąĄą║čéčĆąŠą╗ąĖčéčŗ ą▓ ąĮąĄą╣ ą┤ąĖčüčüąŠčåąĖąĖčĆčāčÄčé ąĮą░ ąĖąŠąĮčŗ. ąÆ ąČąĖą┤ą║ąŠą╣ ą▓ąŠą┤ąĄ ąĮą░čĆčÅą┤čā čü ąŠą▒čŗčćąĮčŗą╝ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░ą╝ąĖ ąØ2ą× čüąŠą┤ąĄčƹȹ░čéčüčÅ ą░čüčüąŠčåąĖąĖčĆąŠą▓ą░ąĮąĮčŗąĄ ą╝ąŠą╗ąĄą║čāą╗čŗ, čé. ąĄ. čüąŠąĄą┤ąĖąĮąĄąĮąĮčŗąĄ ą▓ ą▒ąŠą╗ąĄąĄ čüą╗ąŠąČąĮčŗąĄ ą░ą│čĆąĄą│ą░čéčŗ (ąØ2ą×)čģ, ą▒ą╗ą░ą│ąŠą┤ą░čĆčÅ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÄ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗčģ čüą▓čÅąĘąĄą╣. ąØą░ą╗ąĖčćąĖąĄą╝ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗčģ čüą▓čÅąĘąĄą╣ ą╝ąĄąČą┤čā ą╝ąŠą╗ąĄą║čāą╗ą░ą╝ąĖ ą▓ąŠą┤čŗ ąŠą▒čŖčÅčüąĮčÅčÄčéčüčÅ ą░ąĮąŠą╝ą░ą╗ąĖąĖ ąĄąĄ čäąĖąĘąĖč湥čüą║ąĖčģ čüą▓ąŠą╣čüčéą▓; ą╝ą░ą║čüąĖą╝ą░ą╗čīąĮą░čÅ ą┐ą╗ąŠčéąĮąŠčüčéčī ą┐čĆąĖ 4┬░ ąĪ, ą▓čŗčüąŠą║ą░čÅ č鹥ą╝ą┐ąĄčĆą░čéčāčĆą░ ą║ąĖą┐ąĄąĮąĖčÅ (ą▓ čĆčÅą┤čā ąØ2ą×ŌĆöH2S ŌĆö H2Se ŌĆö ąØ2ąóąĄ), ą░ąĮąŠą╝ą░ą╗čīąĮąŠ ą▓čŗčüąŠą║ą░čÅ č鹥ą┐ą╗ąŠąĄą╝ą║ąŠčüčéčī [4,18 ą║ąöąČ/(ą│ą¦ ąÜ)]. ąĪ ą┐ąŠą▓čŗčłąĄąĮąĖąĄą╝ č鹥ą╝ą┐ąĄčĆą░čéčāčĆčŗ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗąĄ čüą▓čÅąĘąĖ čĆą░ąĘčĆčŗą▓ą░čÄčéčüčÅ, ąĖ ą┐ąŠą╗ąĮčŗą╣ čĆą░ąĘčĆčŗą▓ ąĖčģ ąĮą░čüčéčāą┐ą░ąĄčé ą┐čĆąĖ ą┐ąĄčĆąĄčģąŠą┤ąĄ ą▓ąŠą┤čŗ ą▓ ą┐ą░čĆ.ąźąĖą╝ąĖč湥čüą║ąĖąĄ čüą▓ąŠą╣čüčéą▓ą░. ąÆąŠą┤ą░ ŌĆö ą▓ąĄčüčīą╝ą░ čĆąĄą░ą║čåąĖąŠąĮąĮąŠčüą┐ąŠčüąŠą▒ąĮąŠąĄ ą▓ąĄčēąĄčüčéą▓ąŠ. ą¤čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ ąŠąĮą░ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāąĄčé čüąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ąŠčüąĮąŠą▓ąĮčŗą╝ąĖ ąĖ ą║ąĖčüą╗ąŠčéąĮčŗą╝ąĖ ąŠą║čüąĖą┤ą░ą╝ąĖ, ą░ čéą░ą║ąČąĄ čüąŠ čēąĄą╗ąŠčćąĮčŗą╝ąĖ ąĖ čēąĄą╗ąŠčćąĮąŠąĘąĄą╝ąĄą╗čīąĮčŗą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ: ąÆąŠą┤ą░ ŌĆö ą▓ąĄčüčīą╝ą░ čĆąĄą░ą║čåąĖąŠąĮąĮąŠčüą┐ąŠčüąŠą▒ąĮąŠąĄ ą▓ąĄčēąĄčüčéą▓ąŠ. ą¤čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ ąŠąĮą░ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāąĄčé čüąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ąŠčüąĮąŠą▓ąĮčŗą╝ąĖ ąĖ ą║ąĖčüą╗ąŠčéąĮčŗą╝ąĖ ąŠą║čüąĖą┤ą░ą╝ąĖ, ą░ čéą░ą║ąČąĄ čüąŠ čēąĄą╗ąŠčćąĮčŗą╝ąĖ ąĖ čēąĄą╗ąŠčćąĮąŠąĘąĄą╝ąĄą╗čīąĮčŗą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ: ążąĖąĘąĖč湥čüą║ąĖąĄ čüą▓ąŠą╣čüčéą▓ą░. ą¦ąĖčüčéą░čÅ ą▓ąŠą┤ą░ ą┐čĆąŠąĘčĆą░čćąĮą░, ąĮąĄ ąĖą╝ąĄąĄčé ąĘą░ą┐ą░čģą░ ąĖ ą▓ą║čāčüą░. ąØą░ąĖą▒ąŠą╗čīčłčāčÄ ą┐ą╗ąŠčéąĮąŠčüčéčī ąŠąĮą░ ąĖą╝ąĄąĄčé ą┐čĆąĖ 0 ┬░ąĪ (1 ą│/čüą╝ ą¦ąĖčüčéą░čÅ ą▓ąŠą┤ą░ ą┐čĆąŠąĘčĆą░čćąĮą░, ąĮąĄ ąĖą╝ąĄąĄčé ąĘą░ą┐ą░čģą░ ąĖ ą▓ą║čāčüą░. ąØą░ąĖą▒ąŠą╗čīčłčāčÄ ą┐ą╗ąŠčéąĮąŠčüčéčī ąŠąĮą░ ąĖą╝ąĄąĄčé ą┐čĆąĖ 0 ┬░ąĪ (1 ą│/čüą╝3). ą¤ą╗ąŠčéąĮąŠčüčéčī ą╗čīą┤ą░ ą╝ąĄąĮčīčłąĄ ą┐ą╗ąŠčéąĮąŠčüčéąĖ ąČąĖą┤ą║ąŠą╣ ą▓ąŠą┤čŗ, ą┐ąŠčŹč鹊ą╝čā ą╗ąĄą┤ ą▓čüą┐ą╗čŗą▓ą░ąĄčé ąĮą░ ą┐ąŠą▓ąĄčĆčģąĮąŠčüčéčī. ąÆąŠą┤ą░ ąĘą░ą╝ąĄčƹʹ░ąĄčé ą┐čĆąĖ 0 ┬░ąĪ ąĖ ą║ąĖą┐ąĖčé ą┐čĆąĖ 100┬░ ąĪ ą┐čĆąĖ ą┤ą░ą▓ą╗ąĄąĮąĖąĖ 101 325 ą¤ą░. ą×ąĮą░ ą┐ą╗ąŠčģąŠ ą┐čĆąŠą▓ąŠą┤ąĖčé č鹥ą┐ą╗ąŠčéčā ąĖ ąŠč湥ąĮčī ą┐ą╗ąŠčģąŠ ą┐čĆąŠą▓ąŠą┤ąĖčé 菹╗ąĄą║čéčĆąĖč湥čüčéą▓ąŠ. ąÆąŠą┤ą░ ŌĆö čģąŠčĆąŠčłąĖą╣ čĆą░čüčéą▓ąŠčĆąĖč鹥ą╗čī. ą£ąŠą╗ąĄą║čāą╗ą░ ą▓ąŠą┤čŗ ąĖą╝ąĄąĄčé čāą│ą╗ąŠą▓čāčÄ č乊čĆą╝čā: ą░č鹊ą╝čŗ ą▓ąŠą┤ąŠčĆąŠą┤ą░ ą┐ąŠ ąŠčéąĮąŠčłąĄąĮąĖčÄ ą║ ą║ąĖčüą╗ąŠčĆąŠą┤čā ąŠą▒čĆą░ąĘčāčÄčé čāą│ąŠą╗, čĆą░ą▓ąĮčŗą╣ 104,5┬░. ą¤ąŠčŹč鹊ą╝čā ą╝ąŠą╗ąĄą║čāą╗ą░ ą▓ąŠą┤čŗ ŌĆö ą┤ąĖą┐ąŠą╗čī: čéą░ čćą░čüčéčī ą╝ąŠą╗ąĄą║čāą╗čŗ, ą│ą┤ąĄ ąĮą░čģąŠą┤ąĖčéčüčÅ ą▓ąŠą┤ąŠčĆąŠą┤, ąĘą░čĆčÅąČąĄąĮą░ ą┐ąŠą╗ąŠąČąĖč鹥ą╗čīąĮąŠ, ą░ čćą░čüčéčī, ą│ą┤ąĄ ąĮą░čģąŠą┤ąĖčéčüčÅ ą║ąĖčüą╗ąŠčĆąŠą┤, ŌĆö ąŠčéčĆąĖčåą░č鹥ą╗čīąĮąŠ. ąæą╗ą░ą│ąŠą┤ą░čĆčÅ ą┐ąŠą╗čÅčĆąĮąŠčüčéąĖ ą╝ąŠą╗ąĄą║čāą╗ ą▓ąŠą┤čŗ 菹╗ąĄą║čéčĆąŠą╗ąĖčéčŗ ą▓ ąĮąĄą╣ ą┤ąĖčüčüąŠčåąĖąĖčĆčāčÄčé ąĮą░ ąĖąŠąĮčŗ. ąÆ ąČąĖą┤ą║ąŠą╣ ą▓ąŠą┤ąĄ ąĮą░čĆčÅą┤čā čü ąŠą▒čŗčćąĮčŗą╝ąĖ ą╝ąŠą╗ąĄą║čāą╗ą░ą╝ąĖ ąØ2ą× čüąŠą┤ąĄčƹȹ░čéčüčÅ ą░čüčüąŠčåąĖąĖčĆąŠą▓ą░ąĮąĮčŗąĄ ą╝ąŠą╗ąĄą║čāą╗čŗ, čé. ąĄ. čüąŠąĄą┤ąĖąĮąĄąĮąĮčŗąĄ ą▓ ą▒ąŠą╗ąĄąĄ čüą╗ąŠąČąĮčŗąĄ ą░ą│čĆąĄą│ą░čéčŗ (ąØ2ą×)čģ, ą▒ą╗ą░ą│ąŠą┤ą░čĆčÅ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÄ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗčģ čüą▓čÅąĘąĄą╣. ąØą░ą╗ąĖčćąĖąĄą╝ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗčģ čüą▓čÅąĘąĄą╣ ą╝ąĄąČą┤čā ą╝ąŠą╗ąĄą║čāą╗ą░ą╝ąĖ ą▓ąŠą┤čŗ ąŠą▒čŖčÅčüąĮčÅčÄčéčüčÅ ą░ąĮąŠą╝ą░ą╗ąĖąĖ ąĄąĄ čäąĖąĘąĖč湥čüą║ąĖčģ čüą▓ąŠą╣čüčéą▓; ą╝ą░ą║čüąĖą╝ą░ą╗čīąĮą░čÅ ą┐ą╗ąŠčéąĮąŠčüčéčī ą┐čĆąĖ 4┬░ ąĪ, ą▓čŗčüąŠą║ą░čÅ č鹥ą╝ą┐ąĄčĆą░čéčāčĆą░ ą║ąĖą┐ąĄąĮąĖčÅ (ą▓ čĆčÅą┤čā ąØ2ą×ŌĆöH2S ŌĆö H2Se ŌĆö ąØ2ąóąĄ), ą░ąĮąŠą╝ą░ą╗čīąĮąŠ ą▓čŗčüąŠą║ą░čÅ č鹥ą┐ą╗ąŠąĄą╝ą║ąŠčüčéčī [4,18 ą║ąöąČ/(ą│ą¦ ąÜ)]. ąĪ ą┐ąŠą▓čŗčłąĄąĮąĖąĄą╝ č鹥ą╝ą┐ąĄčĆą░čéčāčĆčŗ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗąĄ čüą▓čÅąĘąĖ čĆą░ąĘčĆčŗą▓ą░čÄčéčüčÅ, ąĖ ą┐ąŠą╗ąĮčŗą╣ čĆą░ąĘčĆčŗą▓ ąĖčģ ąĮą░čüčéčāą┐ą░ąĄčé ą┐čĆąĖ ą┐ąĄčĆąĄčģąŠą┤ąĄ ą▓ąŠą┤čŗ ą▓ ą┐ą░čĆ.ąźąĖą╝ąĖč湥čüą║ąĖąĄ čüą▓ąŠą╣čüčéą▓ą░. ąÆąŠą┤ą░ ŌĆö ą▓ąĄčüčīą╝ą░ čĆąĄą░ą║čåąĖąŠąĮąĮąŠčüą┐ąŠčüąŠą▒ąĮąŠąĄ ą▓ąĄčēąĄčüčéą▓ąŠ. ą¤čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ ąŠąĮą░ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāąĄčé čüąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ąŠčüąĮąŠą▓ąĮčŗą╝ąĖ ąĖ ą║ąĖčüą╗ąŠčéąĮčŗą╝ąĖ ąŠą║čüąĖą┤ą░ą╝ąĖ, ą░ čéą░ą║ąČąĄ čüąŠ čēąĄą╗ąŠčćąĮčŗą╝ąĖ ąĖ čēąĄą╗ąŠčćąĮąŠąĘąĄą╝ąĄą╗čīąĮčŗą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ: ąÆąŠą┤ą░ ŌĆö ą▓ąĄčüčīą╝ą░ čĆąĄą░ą║čåąĖąŠąĮąĮąŠčüą┐ąŠčüąŠą▒ąĮąŠąĄ ą▓ąĄčēąĄčüčéą▓ąŠ. ą¤čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ ąŠąĮą░ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāąĄčé čüąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ąŠčüąĮąŠą▓ąĮčŗą╝ąĖ ąĖ ą║ąĖčüą╗ąŠčéąĮčŗą╝ąĖ ąŠą║čüąĖą┤ą░ą╝ąĖ, ą░ čéą░ą║ąČąĄ čüąŠ čēąĄą╗ąŠčćąĮčŗą╝ąĖ ąĖ čēąĄą╗ąŠčćąĮąŠąĘąĄą╝ąĄą╗čīąĮčŗą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ: 2ą× čüąŠą┤ąĄčƹȹ░čéčüčÅ ą░čüčüąŠčåąĖąĖčĆąŠą▓ą░ąĮąĮčŗąĄ ą╝ąŠą╗ąĄą║čāą╗čŗ, čé. ąĄ. čüąŠąĄą┤ąĖąĮąĄąĮąĮčŗąĄ ą▓ ą▒ąŠą╗ąĄąĄ čüą╗ąŠąČąĮčŗąĄ ą░ą│čĆąĄą│ą░čéčŗ (ąØ2ą×)čģ, ą▒ą╗ą░ą│ąŠą┤ą░čĆčÅ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÄ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗčģ čüą▓čÅąĘąĄą╣. ąØą░ą╗ąĖčćąĖąĄą╝ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗčģ čüą▓čÅąĘąĄą╣ ą╝ąĄąČą┤čā ą╝ąŠą╗ąĄą║čāą╗ą░ą╝ąĖ ą▓ąŠą┤čŗ ąŠą▒čŖčÅčüąĮčÅčÄčéčüčÅ ą░ąĮąŠą╝ą░ą╗ąĖąĖ ąĄąĄ čäąĖąĘąĖč湥čüą║ąĖčģ čüą▓ąŠą╣čüčéą▓; ą╝ą░ą║čüąĖą╝ą░ą╗čīąĮą░čÅ ą┐ą╗ąŠčéąĮąŠčüčéčī ą┐čĆąĖ 4┬░ ąĪ, ą▓čŗčüąŠą║ą░čÅ č鹥ą╝ą┐ąĄčĆą░čéčāčĆą░ ą║ąĖą┐ąĄąĮąĖčÅ (ą▓ čĆčÅą┤čā ąØ2ą×ŌĆöH2S ŌĆö H2Se ŌĆö ąØ2ąóąĄ), ą░ąĮąŠą╝ą░ą╗čīąĮąŠ ą▓čŗčüąŠą║ą░čÅ č鹥ą┐ą╗ąŠąĄą╝ą║ąŠčüčéčī [4,18 ą║ąöąČ/(ą│ą¦ ąÜ)]. ąĪ ą┐ąŠą▓čŗčłąĄąĮąĖąĄą╝ č鹥ą╝ą┐ąĄčĆą░čéčāčĆčŗ ą▓ąŠą┤ąŠčĆąŠą┤ąĮčŗąĄ čüą▓čÅąĘąĖ čĆą░ąĘčĆčŗą▓ą░čÄčéčüčÅ, ąĖ ą┐ąŠą╗ąĮčŗą╣ čĆą░ąĘčĆčŗą▓ ąĖčģ ąĮą░čüčéčāą┐ą░ąĄčé ą┐čĆąĖ ą┐ąĄčĆąĄčģąŠą┤ąĄ ą▓ąŠą┤čŗ ą▓ ą┐ą░čĆ.ąźąĖą╝ąĖč湥čüą║ąĖąĄ čüą▓ąŠą╣čüčéą▓ą░. ąÆąŠą┤ą░ ŌĆö ą▓ąĄčüčīą╝ą░ čĆąĄą░ą║čåąĖąŠąĮąĮąŠčüą┐ąŠčüąŠą▒ąĮąŠąĄ ą▓ąĄčēąĄčüčéą▓ąŠ. ą¤čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ ąŠąĮą░ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāąĄčé čüąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ąŠčüąĮąŠą▓ąĮčŗą╝ąĖ ąĖ ą║ąĖčüą╗ąŠčéąĮčŗą╝ąĖ ąŠą║čüąĖą┤ą░ą╝ąĖ, ą░ čéą░ą║ąČąĄ čüąŠ čēąĄą╗ąŠčćąĮčŗą╝ąĖ ąĖ čēąĄą╗ąŠčćąĮąŠąĘąĄą╝ąĄą╗čīąĮčŗą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ: ąÆąŠą┤ą░ ŌĆö ą▓ąĄčüčīą╝ą░ čĆąĄą░ą║čåąĖąŠąĮąĮąŠčüą┐ąŠčüąŠą▒ąĮąŠąĄ ą▓ąĄčēąĄčüčéą▓ąŠ. ą¤čĆąĖ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ ąŠąĮą░ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāąĄčé čüąŠ ą╝ąĮąŠą│ąĖą╝ąĖ ąŠčüąĮąŠą▓ąĮčŗą╝ąĖ ąĖ ą║ąĖčüą╗ąŠčéąĮčŗą╝ąĖ ąŠą║čüąĖą┤ą░ą╝ąĖ, ą░ čéą░ą║ąČąĄ čüąŠ čēąĄą╗ąŠčćąĮčŗą╝ąĖ ąĖ čēąĄą╗ąŠčćąĮąŠąĘąĄą╝ąĄą╗čīąĮčŗą╝ąĖ ą╝ąĄčéą░ą╗ą╗ą░ą╝ąĖ:  ąÆąŠą┤ą░ ąŠą▒čĆą░ąĘčāąĄčé ą╝ąĮąŠą│ąŠčćąĖčüą╗ąĄąĮąĮčŗąĄ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ŌĆö ą│ąĖą┤čĆą░čéčŗ (ą║čĆąĖčüčéą░ą╗ą╗ąŠą│ąĖą┤čĆą░čéčŗ): 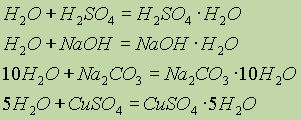 ): 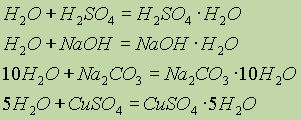 ą×č湥ą▓ąĖą┤ąĮąŠ, čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ, čüą▓čÅąĘčŗą▓ą░čÄčēąĖąĄ ą▓ąŠą┤čā, ą╝ąŠą│čāčé čüą╗čāąČąĖčéčī ą▓ ą║ą░č湥čüčéą▓ąĄ ąŠčüčāčłąĖč鹥ą╗ąĄą╣. ąśąĘ ą┤čĆčāą│ąĖčģ ąŠčüčāčłą░čÄčēąĖčģ ą▓ąĄčēąĄčüčéą▓ ą╝ąŠąČąĮąŠ čāą║ą░ąĘą░čéčī ąĀ2O5O5, ąĪą░ą×, ąÆą░ą×, ą╝ąĄčéą░ą╗ą╗ąĖč湥čüą║ąĖą╣ Na (ąŠąĮąĖ č鹊ąČąĄ čģąĖą╝ąĖč湥čüą║ąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāčÄčé čü ą▓ąŠą┤ąŠą╣), ą░ čéą░ą║ąČąĄ čüąĖą╗ąĖą║ą░ą│ąĄą╗čī.ąÜ ą▓ą░ąČąĮčŗą╝ čģąĖą╝ąĖč湥čüą║ąĖą╝ čüą▓ąŠą╣čüčéą▓ą░ą╝ ą▓ąŠą┤čŗ ąŠčéąĮąŠčüąĖčéčüčÅ ąĄąĄ čüą┐ąŠčüąŠą▒ąĮąŠčüčéčī ą▓čüčéčāą┐ą░čéčī ą▓ čĆąĄą░ą║čåąĖąĖ ą│ąĖą┤čĆąŠą╗ąĖčéąĖč湥čüą║ąŠą│ąŠ čĆą░ąĘą╗ąŠąČąĄąĮąĖčÅ. ąóčÅąČąĄą╗ą░čÅ ą▓ąŠą┤ą░. ąÆąŠą┤ą░, čüąŠą┤ąĄčƹȹ░čēą░čÅ čéčÅąČąĄą╗čŗą╣ ą▓ąŠą┤ąŠčĆąŠą┤, ąĮą░ąĘčŗą▓ą░ąĄčéčüčÅ čéčÅąČąĄą╗ąŠą╣ ą▓ąŠą┤ąŠą╣ (ąŠą▒ąŠąĘąĮą░čćą░ąĄčéčüčÅ č乊čĆą╝čāą╗ąŠą╣ D2O). ąÜą░ą║ čŹč鹊 ą▓ąĖą┤ąĮąŠ ąĖąĘ čüąŠą┐ąŠčüčéą░ą▓ą╗ąĄąĮąĖčÅ čäąĖąĘąĖč湥čüą║ąĖčģ čüą▓ąŠą╣čüčéą▓, ąŠąĮą░ ąŠčéą╗ąĖčćą░ąĄčéčüčÅ ąŠčé ąŠą▒čŗčćąĮąŠą╣ ą▓ąŠą┤čŗ:(ą▓ čüą║ąŠą▒ą║ą░čģ ą┐čĆąĖą▓ąĄą┤ąĄąĮčŗ čģą░čĆą░ą║č鹥čĆąĖčüčéąĖą║ąĖ ąŠą▒čŗčćąĮąŠą╣ ą▓ąŠą┤čŗ (H2O)) 2O5O5, ąĪą░ą×, ąÆą░ą×, ą╝ąĄčéą░ą╗ą╗ąĖč湥čüą║ąĖą╣ Na (ąŠąĮąĖ č鹊ąČąĄ čģąĖą╝ąĖč湥čüą║ąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāčÄčé čü ą▓ąŠą┤ąŠą╣), ą░ čéą░ą║ąČąĄ čüąĖą╗ąĖą║ą░ą│ąĄą╗čī.ąÜ ą▓ą░ąČąĮčŗą╝ čģąĖą╝ąĖč湥čüą║ąĖą╝ čüą▓ąŠą╣čüčéą▓ą░ą╝ ą▓ąŠą┤čŗ ąŠčéąĮąŠčüąĖčéčüčÅ ąĄąĄ čüą┐ąŠčüąŠą▒ąĮąŠčüčéčī ą▓čüčéčāą┐ą░čéčī ą▓ čĆąĄą░ą║čåąĖąĖ ą│ąĖą┤čĆąŠą╗ąĖčéąĖč湥čüą║ąŠą│ąŠ čĆą░ąĘą╗ąŠąČąĄąĮąĖčÅ. ąóčÅąČąĄą╗ą░čÅ ą▓ąŠą┤ą░. ąÆąŠą┤ą░, čüąŠą┤ąĄčƹȹ░čēą░čÅ čéčÅąČąĄą╗čŗą╣ ą▓ąŠą┤ąŠčĆąŠą┤, ąĮą░ąĘčŗą▓ą░ąĄčéčüčÅ čéčÅąČąĄą╗ąŠą╣ ą▓ąŠą┤ąŠą╣ (ąŠą▒ąŠąĘąĮą░čćą░ąĄčéčüčÅ č乊čĆą╝čāą╗ąŠą╣ D2O). ąÜą░ą║ čŹč鹊 ą▓ąĖą┤ąĮąŠ ąĖąĘ čüąŠą┐ąŠčüčéą░ą▓ą╗ąĄąĮąĖčÅ čäąĖąĘąĖč湥čüą║ąĖčģ čüą▓ąŠą╣čüčéą▓, ąŠąĮą░ ąŠčéą╗ąĖčćą░ąĄčéčüčÅ ąŠčé ąŠą▒čŗčćąĮąŠą╣ ą▓ąŠą┤čŗ:(ą▓ čüą║ąŠą▒ą║ą░čģ ą┐čĆąĖą▓ąĄą┤ąĄąĮčŗ čģą░čĆą░ą║č鹥čĆąĖčüčéąĖą║ąĖ ąŠą▒čŗčćąĮąŠą╣ ą▓ąŠą┤čŗ (H2O)) . ąÆąŠą┤ą░, čüąŠą┤ąĄčƹȹ░čēą░čÅ čéčÅąČąĄą╗čŗą╣ ą▓ąŠą┤ąŠčĆąŠą┤, ąĮą░ąĘčŗą▓ą░ąĄčéčüčÅ čéčÅąČąĄą╗ąŠą╣ ą▓ąŠą┤ąŠą╣ (ąŠą▒ąŠąĘąĮą░čćą░ąĄčéčüčÅ č乊čĆą╝čāą╗ąŠą╣ D2O). ąÜą░ą║ čŹč鹊 ą▓ąĖą┤ąĮąŠ ąĖąĘ čüąŠą┐ąŠčüčéą░ą▓ą╗ąĄąĮąĖčÅ čäąĖąĘąĖč湥čüą║ąĖčģ čüą▓ąŠą╣čüčéą▓, ąŠąĮą░ ąŠčéą╗ąĖčćą░ąĄčéčüčÅ ąŠčé ąŠą▒čŗčćąĮąŠą╣ ą▓ąŠą┤čŗ:(ą▓ čüą║ąŠą▒ą║ą░čģ ą┐čĆąĖą▓ąĄą┤ąĄąĮčŗ čģą░čĆą░ą║č鹥čĆąĖčüčéąĖą║ąĖ ąŠą▒čŗčćąĮąŠą╣ ą▓ąŠą┤čŗ (H2O))ą£ąŠą╗ąĄą║čāą╗čÅčĆąĮą░čÅ ą╝ą░čüčüą░: 20 (18) ą¤ą╗ąŠčéąĮąŠčüčéčī ą┐čĆąĖ 20 ┬░ąĪ, ą│/čüą╝3 : 1,1050 (0,9982): 1,1050 (0,9982) ┬░ąĪ, ą│/čüą╝3 : 1,1050 (0,9982): 1,1050 (0,9982)ąóąĄą╝ą┐ąĄčĆą░čéčāčĆą░ ą║čĆąĖčüčéą░ą╗ą╗ąĖąĘą░čåąĖąĖ, oC: 3,8 (0) , oC: 3,8 (0)ąóąĄą╝ą┐ąĄčĆą░čéčāčĆą░ ą║ąĖą┐ąĄąĮąĖčÅ, ┬░ąĪ: 101,4 (100) 101,4 (100) ąźąĖą╝ąĖč湥čüą║ąĖąĄ čĆąĄą░ą║čåąĖąĖ čü čéčÅąČąĄą╗ąŠą╣ ą▓ąŠą┤ąŠą╣ ą┐čĆąŠč鹥ą║ą░čÄčé ąĘąĮą░čćąĖč鹥ą╗čīąĮąŠ ą╝ąĄą┤ą╗ąĄąĮąĮąĄąĄ, č湥ą╝ čü ąŠą▒čŗčćąĮąŠą╣ ą▓ąŠą┤ąŠą╣. ą¤ąŠčŹč鹊ą╝čā ąŠąĮą░ ą┐čĆąĖ ą┤ą╗ąĖč鹥ą╗čīąĮąŠą╝ 菹╗ąĄą║čéčĆąŠą╗ąĖąĘąĄ ąŠą▒čŗčćąĮąŠą╣ ą▓ąŠą┤čŗ ąĮą░ą║ą░ą┐ą╗ąĖą▓ą░ąĄčéčüčÅ ą▓ 菹╗ąĄą║čéčĆąŠą╗ąĖąĘąĄčĆąĄ. ąóčÅąČąĄą╗ą░čÅ ą▓ąŠą┤ą░ ą┐čĆąĖą╝ąĄąĮčÅąĄčéčüčÅ ą▓ ą║ą░č湥čüčéą▓ąĄ ąĘą░ą╝ąĄą┤ą╗ąĖč鹥ą╗ąĄą╣ ąĮąĄą╣čéčĆąŠąĮąŠą▓ ą▓ čÅą┤ąĄčĆąĮčŗčģ čĆąĄą░ą║č鹊čĆą░čģ. |
═Ó°Ķ ĒÓŃÓõ¹:
õĶ’ļŅņ įÕ±“ĶŌÓļ "═ŅŌÓ ąÕÓļ³ĒŅ±“³-2006" ļÓ¾Õ“ 1 ’ÕņĶĶ "ŪŌĖńõ¹ ęÓ“ĒÕ“Ó-2007"
═ÕõÕļ ŅßÓńŅŌÓĒĶ ŌńŅ±ļ¹§-2010
═ÕõÕļ ŅßÓńŅŌÓĒĶ ŌńŅ±ļ¹§-2010 ŽļÓĒ ņÕŅ’Ķ “Ķķ ╦ĶņÕĶĻ±ĻÓ õÕĻļÓÓ÷Ķ V Õ±’¾ßļĶĻÓĒ±ĻĶķ ╚Ē“ÕĒÕ“-’Õõ±ŅŌÕ“ ŽĶĻÓń Ņ ’ŅŌÕõÕĒĶĶ ęÕņ¹ õļ Ņß±¾µõÕĒĶ ŽļÓĒ ’ŅŌÕõÕĒĶ ╠Ó“ÕĶÓļ¹ ¾„Ķ“ÕļÕķ ╬“ “ÕŅĶĶ Ļ ’ÓĻ“ĶĻÕ (ŌĶõÕŅ) 90-ļÕ“ĶÕ ŅßÓńŅŌÓĒĶ ęÓ“Ó±ĻŅķ └ččą ŽÕ±ŅĒÓļĶĶ: ŽÕõ±ÕõÓ“ÕļĶ ’ÓŌĶ“Õļ³±“ŌÓ ŽÕ±ŅĒÓļĶĶ: ═ÓĻŅņ’Ņ±¹ ŽÕ±ŅĒÓļĶĶ: ┬¹õÓ■∙ĶÕ± õÕ “ÕļĶ Ķ±“ŅĶĶ “Ó“Ó±ĻŅŃŅ ĒÓŅõÓ šš Ō. ŽÕ±ŅĒÓļĶĶ: ŽÕõ±ÕõÓ“ÕļĶ ęÓ“ų╚╩Ó Ķ ŽÕńĶõĶ¾ņÓ ┬Õ§ŅŌĒŅŃŅ čŅŌÕ“Ó ę└ččą ŽÕ±ŅĒÓļĶĶ: ŽÕŌ¹Õ ±ÕĻÕ“ÓĶ ęÓ“Ó±ĻŅŃŅ ŅßĻŅņÓ, Õ±ĻŅņÓ ’Ó“ĶĶ ╚±“ŅĶ : Ņ¶Ķ÷ĶÓļ³Ē¹Õ õŅĻ¾ņÕĒ“¹ ┬Õ§Ķ Ķ±“ŅĶĶ šŅĒĶĻÓ Ķ±“ŅĶĶ ę└ččą įŅ“ŅŃÓ¶ĶĶ ŽŅ¶Ķļ³ĒŅÕ Ņß¾„ÕĒĶÕ Ō ±ÕõĒÕķ °ĻŅļÕ čŅõÕµÓĒĶÕ Ķ ±Ņ’ŅŌŅµõÕĒĶÕ ═ŅņÓ“ĶŌĒŅÕ ŅßÕ±’Õ„ÕĒĶÕ įŅņ¹ Ķ“ŅŃŅŌŅķ Ó““Õ±“Ó÷ĶĶ ╠ÕŅ’Ķ “Ķ įŅ¾ņ¹ 2010 ąÓ±’Ķ±ÓĒĶÕ ¶Ņ¾ņŅŌ ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ņÓ“ÕņÓ“ĶĻÕ ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ¾±±ĻŅņ¾ ń¹Ļ¾ ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ßĶŅļŅŃĶĶ Ķ §ĶņĶĶ ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ¶ĶńĶĻÕ (16 - 17 ¶ÕŌÓļ 2010 Ń.) ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ĶĒŅ±“ÓĒĒ¹ņ ń¹ĻÓņ (25 - 26 ¶ÕŌÓļ 2010 Ń.) ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ĶĒ¶ŅņÓ“ĶĻÕ (2 - 3 ņÓ“Ó 2010 Ń.) ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ŃÕŅŃÓ¶ĶĶ (4 - 5 ņÓ“Ó 2010 Ń.) Ų¾ĒÓļ "╚Ē¶ŅņÓ“ĶńÓ÷Ķ ŅßÓńŅŌÓĒĶ . ŽŅßļÕņ¹ Ķ ’ŅĶ±ĻĶ" č“Ó“³Ķ µ¾ĒÓļÓ "╚Ē¶ŅņÓ“ĶńÓ÷Ķ ŅßÓńŅŌÓĒĶ . ŽŅßļÕņ¹ Ķ ’ŅĶ±ĻĶ" Ž¾ßļĶ„Ē¹Õ ļÕĻ÷ĶĶ ╬ß∙Ó ĶĒ¶ŅņÓ÷Ķ 2007/2008 2008/2009 2009/2010 III Ņ“Ļ¹“¹ķ ĻŅĒĻ¾± ĶĒ“ÕĒÕ“ ±Óķ“ŅŌ čÓķ“¹-¾„Ó±“ĒĶĻĶ ŽĶĻÓń Ņ ’ŅŌÕõÕĒĶĶ ╠ÕŅ’Ķ “Ķ ąÕ±’¾ßļĶĻÓĒ±ĻŅÕ ÓŌŃ¾±“ŅŌ±ĻŅÕ ±ŅŌÕ∙ÓĒĶÕ ÓßŅ“ĒĶĻŅŌ ŅßÓńŅŌÓĒĶ Ķ ĒÓ¾ĻĶ 2009 IV ąÕ±’¾ßļĶĻÓĒ±ĻĶķ ╚Ē“ÕĒÕ“-’Õõ±ŅŌÕ“ IV ąÕ±’¾ßļĶĻÓĒ±ĻŅķ ĶĒ“ÕĒÕ“-ÓĻ÷Ķ "═ÕõÕļ ŅßÓńŅŌÓĒĶ ŌńŅ±ļ¹§" ╚Ē¶ŅņÓ÷Ķ Ņ ĒÕõÕļÕ ŅßÓńŅŌÓĒĶ ŌńŅ±ļ¹§ ŽŅŌ¹°ÕĒĶÕ ĻŌÓļĶ¶ĶĻÓ÷ĶĶ ’Ņ ╚╩ę ═Ņ¾“ß¾Ļ ¾„Ķ“Õļ . ╬±ĒŅŌ¹ ÓßŅ“¹ ŽŅŃÓņņÓ Intel "╬ß¾„ÕĒĶÕ õļ ß¾õ¾∙ÕŃŅ" ŽŅŃÓņņÓ "ė„Ķņ± ± Intel" ╩ÓļÕķõŅ±ĻŅ’ 

|
|