 |
 |
| ├ļÓŌĒÓ | ęÕ±“¹ ┼├▌ | ╩ĒĶŃĶ | ąÕ±¾±¹ | ┬Õß-ĻÓ“ÓļŅŃ | įŅ¾ņ | ╬ ’Ņ“ÓļÕ |
±ÕŃŅõĒ : ’ “ĒĶ÷Ó, 3 ņÓ 2024
|
||||||||||||
±ÕŃŅõĒ : ’ “ĒĶ÷Ó, 3 ņÓ 2024
|
||||||||||||
|
▌ļÕĻ“ŅĒĒÓ ßĶßļĶŅ“ÕĻÓ
ą£ą░čĆą│ą░ąĮąĄčå
ąØąĢą×ąĀąōąÉąØąśą¦ąĢąĪąÜąÉą» ąźąśą£ąśą». ąŁąøąĢą£ąĢąØąóą½ ąś ąśąź ąĪą×ąĢąöąśąØąĢąØąśą»17. ą£ą░čĆą│ą░ąĮąĄčåąĪą▓ąŠą╣čüčéą▓ą░ 菹╗ąĄą╝ąĄąĮč鹊ą▓ VII B ą│čĆčāą┐ą┐čŗ.
ą£ą░čĆą│ą░ąĮąĄčå. ą£ąĄčéą░ą╗ą╗ąĖč湥čüą║ąĖą╣ ą╝ą░čĆą│ą░ąĮąĄčå čĆąĄą░ą│ąĖčĆčāąĄčé čü ą║ąĖčüą╗ąŠčéą░ą╝ąĖ, ąŠą▒čĆą░ąĘčāčÅ čüąŠą╗ąĖ ą╝ą░čĆą│ą░ąĮčåą░ (II): (II): ą£ąĄčéą░ą╗ą╗ąĖč湥čüą║ąĖą╣ ą╝ą░čĆą│ą░ąĮąĄčå čĆąĄą░ą│ąĖčĆčāąĄčé čü ą║ąĖčüą╗ąŠčéą░ą╝ąĖ, ąŠą▒čĆą░ąĘčāčÅ čüąŠą╗ąĖ ą╝ą░čĆą│ą░ąĮčåą░ (II): (II): ąÆ čĆą░ąĘą╗ąĖčćąĮčŗčģ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅčģ ą╝ą░čĆą│ą░ąĮąĄčå ą┐čĆąŠčÅą▓ą╗čÅąĄčé čüč鹥ą┐ąĄąĮąĖ ąŠą║ąĖčüą╗ąĄąĮąĖčÅ 2+, 4+, 6+ ąĖ 7+. ą¦ąĄą╝ ą▓čŗčłąĄ čüč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ, č鹥ą╝ ą▒ąŠą╗ąĄąĄ ą║ąŠą▓ą░ą╗ąĄąĮčéąĮčŗą╣ čģą░čĆą░ą║č鹥čĆ ąĖą╝ąĄčÄčé čüąŠąŠčéą▓ąĄčéčüčéą▓čāčÄčēąĖąĄ čüąŠąĄą┤ąĖąĮąĄąĮąĖčÅ. ąĪ ą▓ąŠąĘčĆą░čüčéą░ąĮąĖąĄą╝ čüč鹥ą┐ąĄąĮąĖ ąŠą║ąĖčüą╗ąĄąĮąĖčÅ ą╝ą░čĆą│ą░ąĮčåą░ čāą▓ąĄą╗ąĖčćąĖą▓ą░ąĄčéčüčÅ čéą░ą║ąČąĄ ą║ąĖčüą╗ąŠčéąĮąŠčüčéčī ąĄą│ąŠ ąŠą║čüąĖą┤ąŠą▓. ą¤čĆąĖ ąĮą░ą│čĆąĄą▓ą░ąĮąĖąĖ ą╝ą░čĆą│ą░ąĮąĄčå ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāąĄčé čü ą║ąĖčüą╗ąŠčĆąŠą┤ąŠą╝, ą│ą░ą╗ąŠą│ąĄąĮą░ą╝ąĖ, čāą│ą╗ąĄčĆąŠą┤ąŠą╝, ą▒ąŠčĆąŠą╝, ą║čĆąĄą╝ąĮąĖąĄą╝, čüąĄčĆąŠą╣. ą¤čĆąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĖ ą╝ą░čĆą│ą░ąĮčåą░ čü ą║ąĖčüą╗ąŠčĆąŠą┤ąŠą╝ ąŠą▒čĆą░ąĘčāčÄčéčüčÅ čüą╝ąĄčłą░ąĮąĮčŗąĄ ąŠą║čüąĖą┤čŗ: ąöąĖčüą┐ąĄčĆą│ąĖčĆąŠą▓ą░ąĮąĮčŗą╣ ą╝ą░čĆą│ą░ąĮąĄčå ą┐čĆąĖ ąĮą░ą│čĆąĄą▓ą░ąĮąĖąĖ čĆąĄą░ą│ąĖčĆčāąĄčé čü ą▓ąŠą┤ąŠą╣: ą×ą┤ąĮąŠą╣ ąĖąĘ ąŠčüąŠą▒ąĄąĮąĮąŠčüč鹥ą╣ ą╝ą░čĆą│ą░ąĮčåą░ čÅą▓ą╗čÅąĄčéčüčÅ čüą┐ąŠčüąŠą▒ąĮąŠčüčéčī ą┐ąŠą│ą╗ąŠčēą░čéčī ą║ąĖčüą╗ąŠčĆąŠą┤. ą£ą░čĆą│ą░ąĮąĄčå ą┐ą░čüčüąĖą▓ąĖčĆčāąĄčéčüčÅ ą▓ ąŠą▒čŗčćąĮčŗčģ čāčüą╗ąŠą▓ąĖčÅčģ ą║ąŠąĮčåąĄąĮčéčĆąĖčĆąŠą▓ą░ąĮąĮčŗą╝ąĖ ą║ąĖčüą╗ąŠčéą░ą╝ąĖ ąŠą║ąĖčüą╗ąĖč鹥ą╗čÅą╝ąĖ, čģąŠčéčÅ ą┐čĆąĖ ąĮą░ą│čĆąĄą▓ą░ąĮąĖąĖ čĆąĄą░ą║čåąĖčÅ ąĖą┤ąĄčé: ą¤čĆąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĖ čü čĆą░ąĘą▒ą░ą▓ą╗ąĄąĮąĮčŗą╝ąĖ ą║ąĖčüą╗ąŠčéą░ą╝ąĖ ą▓čŗą┤ąĄą╗čÅąĄčéčüčÅ ą▓ąŠą┤ąŠčĆąŠą┤: ąØą░ čüą░ą╝ąŠą╝ ą┤ąĄą╗ąĄ ą▓ čĆą░čüčéą▓ąŠčĆąĄ čüčāčēąĄčüčéą▓čāąĄčé ą░ą║ą▓ą░ą║ąŠą╝ą┐ą╗ąĄą║čü [Mn(H2O)6]Cl2. [Mn(H2O)6]Cl2.ą£ą░čĆą│ą░ąĮąĄčå ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓čāąĄčé čüąŠ čēąĄą╗ąŠčćą░ą╝ąĖ ą▓ ą┐čĆąĖčüčāčéčüčéą▓ąĖąĄ ąŠą║ąĖčüą╗ąĖč鹥ą╗čÅ: ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (II). ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (II) ą╝ąŠąČąĮąŠ ą┐ąŠą╗čāčćąĖčéčī ą▓ąŠčüčüčéą░ąĮąŠą▓ą╗ąĄąĮąĖąĄ ąŠą║čüąĖą┤ą░ ą╝ą░čĆą│ą░ąĮčåą░ (IV): II). ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (II) ą╝ąŠąČąĮąŠ ą┐ąŠą╗čāčćąĖčéčī ą▓ąŠčüčüčéą░ąĮąŠą▓ą╗ąĄąĮąĖąĄ ąŠą║čüąĖą┤ą░ ą╝ą░čĆą│ą░ąĮčåą░ (IV): ąŁč鹊čé ąŠą║čüąĖą┤ ąŠą▒ą╗ą░ą┤ą░ąĄčé ąŠčüąĮąŠą▓ąĮčŗą╝ąĖ čüą▓ąŠą╣čüčéą▓ą░ą╝ąĖ. ąóą░ą║, ąŠąĮ ąĮąĄ čĆąĄą░ą│ąĖčĆčāąĄčé čü ą▓ąŠą┤ąŠą╣, ą░ ą┐čĆąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĖ čü ą║ąĖčüą╗ąŠčéą░ą╝ąĖ ąŠą▒čĆą░ąĘčāčÄčéčüčÅ čüąŠą╗ąĖ ą╝ą░čĆą│ą░ąĮčåą░ (II): II): ąōąĖą┤čĆąŠą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (II). ą¤čĆąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĖ čüąŠą╗ąĄą╣ ą╝ą░čĆą│ą░ąĮčåą░ (II) čüąŠ čēąĄą╗ąŠčćą░ą╝ąĖ ą▓čŗą┐ą░ą┤ą░ąĄčé ą▒ąĄą╗čŗą╣, ąĮąĄčĆą░čüčéą▓ąŠčĆąĖą╝čŗą╣ ąŠčüą░ą┤ąŠą║ Mn(OH)2: II). ą¤čĆąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĖ čüąŠą╗ąĄą╣ ą╝ą░čĆą│ą░ąĮčåą░ (II) čüąŠ čēąĄą╗ąŠčćą░ą╝ąĖ ą▓čŗą┐ą░ą┤ą░ąĄčé ą▒ąĄą╗čŗą╣, ąĮąĄčĆą░čüčéą▓ąŠčĆąĖą╝čŗą╣ ąŠčüą░ą┤ąŠą║ Mn(OH)2: ą¤čĆąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĖ čü ą║ąĖcą╗ąŠčéą░ą╝ąĖ ąŠčé ą┤ą░ąĄčé čüąŠą╗ąĖ ą╝ą░čĆą│ą░ąĮčåą░ (II): cą╗ąŠčéą░ą╝ąĖ ąŠčé ą┤ą░ąĄčé čüąŠą╗ąĖ ą╝ą░čĆą│ą░ąĮčåą░ (II): ą¤čĆąĖ čüč鹊čÅąĮąĖąĖ ąĮą░ ą▓ąŠąĘą┤čāčģąĄ ą│ąĖą┤čĆąŠą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (II) ą┐ąĄčĆąĄčģąŠą┤ąĖčé ą▓ ąŠą║čüąŠą│ąĖą┤čĆąŠą║čüąĖą┤, ą║ąŠč鹊čĆčŗą╣ ą┤ą░ą╗ąĄąĄ ąŠą║ąĖčüą╗čÅąĄčéčüčÅ ą┤ąŠ ąŠą║čüąĖą┤ą░ ą╝ą░čĆą│ą░ąĮčåą░ (IV):  II) ą┐ąĄčĆąĄčģąŠą┤ąĖčé ą▓ ąŠą║čüąŠą│ąĖą┤čĆąŠą║čüąĖą┤, ą║ąŠč鹊čĆčŗą╣ ą┤ą░ą╗ąĄąĄ ąŠą║ąĖčüą╗čÅąĄčéčüčÅ ą┤ąŠ ąŠą║čüąĖą┤ą░ ą╝ą░čĆą│ą░ąĮčåą░ (IV):  ąÉąĮą░ą╗ąŠą│ąĖčćąĮą░čÅ čĆąĄą░ą║čåąĖčÅ ą┐čĆąŠč鹥ą║ą░ąĄčé čü čüčāą╗čīčäąĖą┤ąŠą╝ ą╝ą░čĆą│ą░ąĮčåą░ MnS, ąĮąŠ čü ą▓čŗą┐ą░ą┤ąĄąĮąĖąĄą╝ ąŠčüą░ą┤ą║ą░ čüąĄčĆčŗ. ąĪąŠą╗ąĖ ą╝ą░čĆą│ą░ąĮčåą░ (II). ą£ą░čĆą│ą░ąĮąĄčå (II) ą┐čĆąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĖ čü čüąĖą╗čīąĮčŗą╝ąĖ ąŠą║ąĖčüą╗ąĖč鹥ą╗čÅą╝ąĖ ą┐ąĄčĆąĄčģąŠą┤ąĖčé ą▓ čĆą░ąĘą╗ąĖčćąĮčŗąĄ čüč鹥ą┐ąĄąĮąĖ ąŠą║ąĖčüą╗ąĄąĮąĖčÅ ą▓ ąĘą░ą▓ąĖčüąĖą╝ąŠčüčéąĖ ąŠčé čĆąĄą░ą║čåąĖąĖ čüčĆąĄą┤čŗ: ą£ą░čĆą│ą░ąĮąĄčå (II) ą┐čĆąĖ ą▓ąĘą░ąĖą╝ąŠą┤ąĄą╣čüčéą▓ąĖąĖ čü čüąĖą╗čīąĮčŗą╝ąĖ ąŠą║ąĖčüą╗ąĖč鹥ą╗čÅą╝ąĖ ą┐ąĄčĆąĄčģąŠą┤ąĖčé ą▓ čĆą░ąĘą╗ąĖčćąĮčŗąĄ čüč鹥ą┐ąĄąĮąĖ ąŠą║ąĖčüą╗ąĄąĮąĖčÅ ą▓ ąĘą░ą▓ąĖčüąĖą╝ąŠčüčéąĖ ąŠčé čĆąĄą░ą║čåąĖąĖ čüčĆąĄą┤čŗ: 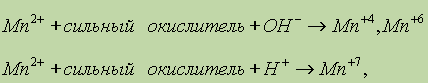 čćč鹊 ą╝ąŠąČąĮąŠ ą┐čĆąŠąĖą╗ą╗čÄčüčéčĆąĖčĆąŠą▓ą░čéčī čüą╗ąĄą┤čāčÄčēąĖą╝ąĖ ą┐čĆąĖą╝ąĄčĆą░ą╝ąĖ: 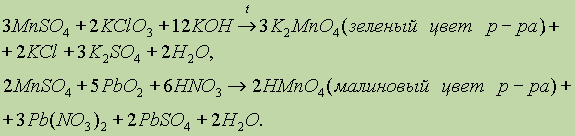 ąÜ čéčĆčāą┤ąĮąŠ čĆą░čüčéą▓ąŠčĆąĖą╝čŗą╝ čüąŠą╗čÅą╝ ą╝ą░čĆą│ą░ąĮčåą░ (II) ąŠčéąĮąŠčüčÅčéčüčÅ čäč鹊čĆąĖą┤, ą║ą░čĆą▒ąŠąĮą░čé ąĖ č乊čüčäą░čé.ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (IV). ąØą░ąĖą▒ąŠą╗ąĄąĄ ą▓ą░ąČąĮčŗą╝ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄą╝ ą╝ą░čĆą│ą░ąĮčåą░ (IV) čÅą▓ą╗čÅąĄčéčüčÅ ąĄą│ąŠ ąŠą║čüąĖą┤ MnO2. ąŁč鹊 čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ą║ąŠčĆąĖčćąĮąĄą▓ąŠ-č湥čĆąĮąŠą│ąŠ čåą▓ąĄčéą░ ąĮąĄ čĆą░čüčéą▓ąŠčĆčÅąĄčéčüčÅ ą▓ ą▓ąŠą┤ąĄ. ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (IV) ŌĆö čüąĖą╗čīąĮčŗą╣ ąŠą║ąĖčüą╗ąĖč鹥ą╗čī, ą║ąŠč鹊čĆčŗą╣, ąĮą░ą┐čĆąĖą╝ąĄčĆ, ąŠą║ąĖčüą╗čÅąĄčé ą║ąŠąĮčåąĄąĮčéčĆąĖčĆąŠą▓ą░ąĮąĮčāčÄ čüąŠą╗čÅąĮčāčÄ ą║ąĖčüą╗ąŠčéčā ą┤ąŠ čģą╗ąŠčĆą░: ąÜ čéčĆčāą┤ąĮąŠ čĆą░čüčéą▓ąŠčĆąĖą╝čŗą╝ čüąŠą╗čÅą╝ ą╝ą░čĆą│ą░ąĮčåą░ (II) ąŠčéąĮąŠčüčÅčéčüčÅ čäč鹊čĆąĖą┤, ą║ą░čĆą▒ąŠąĮą░čé ąĖ č乊čüčäą░čé.ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (IV). ąØą░ąĖą▒ąŠą╗ąĄąĄ ą▓ą░ąČąĮčŗą╝ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄą╝ ą╝ą░čĆą│ą░ąĮčåą░ (IV) čÅą▓ą╗čÅąĄčéčüčÅ ąĄą│ąŠ ąŠą║čüąĖą┤ MnO2. ąŁč鹊 čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ą║ąŠčĆąĖčćąĮąĄą▓ąŠ-č湥čĆąĮąŠą│ąŠ čåą▓ąĄčéą░ ąĮąĄ čĆą░čüčéą▓ąŠčĆčÅąĄčéčüčÅ ą▓ ą▓ąŠą┤ąĄ. ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (IV) ŌĆö čüąĖą╗čīąĮčŗą╣ ąŠą║ąĖčüą╗ąĖč鹥ą╗čī, ą║ąŠč鹊čĆčŗą╣, ąĮą░ą┐čĆąĖą╝ąĄčĆ, ąŠą║ąĖčüą╗čÅąĄčé ą║ąŠąĮčåąĄąĮčéčĆąĖčĆąŠą▓ą░ąĮąĮčāčÄ čüąŠą╗čÅąĮčāčÄ ą║ąĖčüą╗ąŠčéčā ą┤ąŠ čģą╗ąŠčĆą░:ąÜ čéčĆčāą┤ąĮąŠ čĆą░čüčéą▓ąŠčĆąĖą╝čŗą╝ čüąŠą╗čÅą╝ ą╝ą░čĆą│ą░ąĮčåą░ (II) ąŠčéąĮąŠčüčÅčéčüčÅ čäč鹊čĆąĖą┤, ą║ą░čĆą▒ąŠąĮą░čé ąĖ č乊čüčäą░čé.ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (IV). ąØą░ąĖą▒ąŠą╗ąĄąĄ ą▓ą░ąČąĮčŗą╝ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄą╝ ą╝ą░čĆą│ą░ąĮčåą░ (IV) čÅą▓ą╗čÅąĄčéčüčÅ ąĄą│ąŠ ąŠą║čüąĖą┤ MnO2. ąŁč鹊 čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ą║ąŠčĆąĖčćąĮąĄą▓ąŠ-č湥čĆąĮąŠą│ąŠ čåą▓ąĄčéą░ ąĮąĄ čĆą░čüčéą▓ąŠčĆčÅąĄčéčüčÅ ą▓ ą▓ąŠą┤ąĄ. ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (IV) ŌĆö čüąĖą╗čīąĮčŗą╣ ąŠą║ąĖčüą╗ąĖč鹥ą╗čī, ą║ąŠč鹊čĆčŗą╣, ąĮą░ą┐čĆąĖą╝ąĄčĆ, ąŠą║ąĖčüą╗čÅąĄčé ą║ąŠąĮčåąĄąĮčéčĆąĖčĆąŠą▓ą░ąĮąĮčāčÄ čüąŠą╗čÅąĮčāčÄ ą║ąĖčüą╗ąŠčéčā ą┤ąŠ čģą╗ąŠčĆą░: IV). ąØą░ąĖą▒ąŠą╗ąĄąĄ ą▓ą░ąČąĮčŗą╝ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄą╝ ą╝ą░čĆą│ą░ąĮčåą░ (IV) čÅą▓ą╗čÅąĄčéčüčÅ ąĄą│ąŠ ąŠą║čüąĖą┤ MnO2. ąŁč鹊 čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ą║ąŠčĆąĖčćąĮąĄą▓ąŠ-č湥čĆąĮąŠą│ąŠ čåą▓ąĄčéą░ ąĮąĄ čĆą░čüčéą▓ąŠčĆčÅąĄčéčüčÅ ą▓ ą▓ąŠą┤ąĄ. ą×ą║čüąĖą┤ ą╝ą░čĆą│ą░ąĮčåą░ (IV) ŌĆö čüąĖą╗čīąĮčŗą╣ ąŠą║ąĖčüą╗ąĖč鹥ą╗čī, ą║ąŠč鹊čĆčŗą╣, ąĮą░ą┐čĆąĖą╝ąĄčĆ, ąŠą║ąĖčüą╗čÅąĄčé ą║ąŠąĮčåąĄąĮčéčĆąĖčĆąŠą▓ą░ąĮąĮčāčÄ čüąŠą╗čÅąĮčāčÄ ą║ąĖčüą╗ąŠčéčā ą┤ąŠ čģą╗ąŠčĆą░: ąŁčéą░ čĆąĄą░ą║čåąĖčÅ čćą░čüč鹊 ąĖčüą┐ąŠą╗čīąĘčāąĄčéčüčÅ ą┤ą╗čÅ ą┐ąŠą╗čāč湥ąĮąĖčÅ čģą╗ąŠčĆą░ ą▓ ą╗ą░ą▒ąŠčĆą░č鹊čĆąĖąĖ. ąŁč鹊čé ąŠą║čüąĖą┤ ąŠą▒ą╗ą░ą┤ą░ąĄčé ą░ą╝č乊č鹥čĆąĮčŗą╝ąĖ čüą▓ąŠą╣čüčéą▓ą░ą╝ąĖ, čĆą░ą▓ąĮąŠ ą║ą░ą║ ąĖ ąŠą║čüąŠą│ąĖą┤čĆąŠą║čüąĖą┤ MnO(OH)2 ąĖ ą│ąĖą┤čĆąŠą║čüąĖą┤ Mn(OH)4 ą╝ą░čĆą│ą░ąĮčåą░ (IV): MnO(OH)2 ąĖ ą│ąĖą┤čĆąŠą║čüąĖą┤ Mn(OH)4 ą╝ą░čĆą│ą░ąĮčåą░ (IV): ą£ą░ąĮą│ą░ąĮą░čé ą║ą░ą╗ąĖčÅ. ąĪąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą╝ą░čĆą│ą░ąĮčåą░ (VI) ą╝ą░ą╗ąŠčāčüč鹊ą╣čćąĖą▓čŗ, ąŠą┤ąĮą░ą║ąŠ ąĮą░ąĖą▒ąŠą╗ąĄąĄ ąĖąĘą▓ąĄčüčéąĮąŠąĄ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ŌĆö ą╝ą░ąĮą│ą░ąĮą░čé ą║ą░ą╗ąĖčÅ K2Mną×4 ŌĆö ŌĆö čāčüč鹊ą╣čćąĖą▓ ą▓ čēąĄą╗ąŠčćąĮąŠą╣ čüčĆąĄą┤ąĄ. ą×ąĮ ąŠą▒čĆą░ąĘčāąĄčéčüčÅ ą┐čĆąĖ ą▓ąŠčüčüčéą░ąĮąŠą▓ą╗ąĄąĮąĖąĖ ą┐ąĄčĆą╝ą░ąĮą│ą░ąĮą░čéą░ ą║ą░ą╗ąĖčÅ ą▓ čēąĄą╗ąŠčćąĮąŠą╣ čüčĆąĄą┤ąĄ, ąĮą░ą┐čĆąĖą╝ąĄčĆ: ąĪąŠąĄą┤ąĖąĮąĄąĮąĖčÅ ą╝ą░čĆą│ą░ąĮčåą░ (VI) ą╝ą░ą╗ąŠčāčüč鹊ą╣čćąĖą▓čŗ, ąŠą┤ąĮą░ą║ąŠ ąĮą░ąĖą▒ąŠą╗ąĄąĄ ąĖąĘą▓ąĄčüčéąĮąŠąĄ čüąŠąĄą┤ąĖąĮąĄąĮąĖąĄ ŌĆö ą╝ą░ąĮą│ą░ąĮą░čé ą║ą░ą╗ąĖčÅ K2Mną×4 ŌĆö ŌĆö čāčüč鹊ą╣čćąĖą▓ ą▓ čēąĄą╗ąŠčćąĮąŠą╣ čüčĆąĄą┤ąĄ. ą×ąĮ ąŠą▒čĆą░ąĘčāąĄčéčüčÅ ą┐čĆąĖ ą▓ąŠčüčüčéą░ąĮąŠą▓ą╗ąĄąĮąĖąĖ ą┐ąĄčĆą╝ą░ąĮą│ą░ąĮą░čéą░ ą║ą░ą╗ąĖčÅ ą▓ čēąĄą╗ąŠčćąĮąŠą╣ čüčĆąĄą┤ąĄ, ąĮą░ą┐čĆąĖą╝ąĄčĆ: ąÆąŠąŠą▒čēąĄ ą┤ą╗čÅ Mn6+ čģą░čĆą░ą║č鹥čĆąĮčŗ čüą╗ąĄą┤čāčÄčēąĖąĄ ą┐čĆąŠą┤čāą║čéčŗ ąŠą║ąĖčüą╗ąĖč鹥ą╗čīąĮąŠ-ą▓ąŠčüčüčéą░ąĮąŠą▓ąĖč鹥ą╗čīąĮčŗčģ čĆąĄą░ą║čåąĖą╣: Mn6+ čģą░čĆą░ą║č鹥čĆąĮčŗ čüą╗ąĄą┤čāčÄčēąĖąĄ ą┐čĆąŠą┤čāą║čéčŗ ąŠą║ąĖčüą╗ąĖč鹥ą╗čīąĮąŠ-ą▓ąŠčüčüčéą░ąĮąŠą▓ąĖč鹥ą╗čīąĮčŗčģ čĆąĄą░ą║čåąĖą╣: 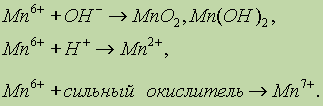 ąØą░ą┐čĆąĖą╝ąĄčĆ: ąÆčŗčüčłčāčÄ čüč鹥ą┐ąĄąĮčī ąŠą║ąĖčüą╗ąĄąĮąĖčÅ 7+ ą╝ą░čĆą│ą░ąĮąĄčå ąĖą╝ąĄąĄčé ą▓ ą║ąĖčüą╗ąŠčéąĮąŠą╝ ąŠą║čüąĖą┤ąĄ ą£n2ą×7 ąĖ ą┐ąĄčĆą╝ą░ąĮą│ą░ąĮą░č鹥 ą║ą░ą╗ąĖčÅ ąÜą╝nO4. ą¤ąŠčüą╗ąĄą┤ąĮąĄąĄ ą▓ąĄčēąĄčüčéą▓ąŠ ŌĆö ą║čĆąĖčüčéą░ą╗ą╗čŗ čäąĖąŠą╗ąĄč鹊ą▓ąŠą│ąŠ čåą▓ąĄčéą░, čģąŠčĆąŠčłąŠ čĆą░čüčéą▓ąŠčĆąĖą╝čŗąĄ ą▓ ą▓ąŠą┤ąĄ.ą¤ąĄčĆą╝ą░ąĮą│ą░ąĮą░čé ą║ą░ą╗ąĖčÅ ŌĆö čüąĖą╗čīąĮąĄą╣čłąĖą╣ ąŠą║ąĖčüą╗ąĖč鹥ą╗čī. ąÆ ą║ąĖčüą╗ąŠą╣ čüčĆąĄą┤ąĄ ąŠąĮ ą▓ąŠčüčüčéą░ąĮą░ą▓ą╗ąĖą▓ą░ąĄčéčüčÅ ą┤ąŠ ąĖąŠąĮąŠą▓ ą£ čüčĆąĄą┤ąĄ ąŠąĮ ą▓ąŠčüčüčéą░ąĮą░ą▓ą╗ąĖą▓ą░ąĄčéčüčÅ ą┤ąŠ ąĖąŠąĮąŠą▓ ą£n2+: ąÆ ą║ąĖčüą╗ąŠą╣ čüčĆąĄą┤ąĄ ąŠąĮ ą▓ąŠčüčüčéą░ąĮą░ą▓ą╗ąĖą▓ą░ąĄčéčüčÅ ą┤ąŠ ąĖąŠąĮąŠą▓ ą£ čüčĆąĄą┤ąĄ ąŠąĮ ą▓ąŠčüčüčéą░ąĮą░ą▓ą╗ąĖą▓ą░ąĄčéčüčÅ ą┤ąŠ ąĖąŠąĮąŠą▓ ą£n2+: ą▓ čēąĄą╗ąŠčćąĮąŠą╣ čüčĆąĄą┤ąĄ ŌĆö ą┤ąŠ ąÜ2ą£nO4 (čüą╝. ą▓čŗčłąĄ), ą░ ą▓ ąĮąĄą╣čéčĆą░ą╗čīąĮąŠą╣ čüčĆąĄą┤ąĄ ŌĆö ą┤ąŠ MnO2: 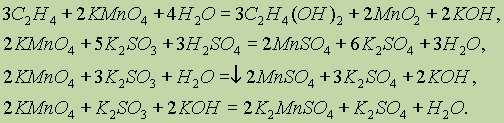 čüčĆąĄą┤ąĄ ŌĆö ą┤ąŠ ąÜ2ą£nO4 (čüą╝. ą▓čŗčłąĄ), ą░ ą▓ ąĮąĄą╣čéčĆą░ą╗čīąĮąŠą╣ čüčĆąĄą┤ąĄ ŌĆö ą┤ąŠ MnO2: 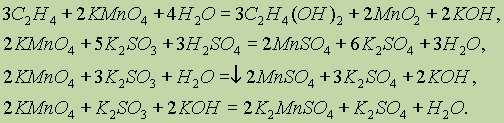 |
═Ó°Ķ ĒÓŃÓõ¹:
õĶ’ļŅņ įÕ±“ĶŌÓļ "═ŅŌÓ ąÕÓļ³ĒŅ±“³-2006" ļÓ¾Õ“ 1 ’ÕņĶĶ "ŪŌĖńõ¹ ęÓ“ĒÕ“Ó-2007"
═ÕõÕļ ŅßÓńŅŌÓĒĶ ŌńŅ±ļ¹§-2010
═ÕõÕļ ŅßÓńŅŌÓĒĶ ŌńŅ±ļ¹§-2010 ŽļÓĒ ņÕŅ’Ķ “Ķķ ╦ĶņÕĶĻ±ĻÓ õÕĻļÓÓ÷Ķ V Õ±’¾ßļĶĻÓĒ±ĻĶķ ╚Ē“ÕĒÕ“-’Õõ±ŅŌÕ“ ŽĶĻÓń Ņ ’ŅŌÕõÕĒĶĶ ęÕņ¹ õļ Ņß±¾µõÕĒĶ ŽļÓĒ ’ŅŌÕõÕĒĶ ╠Ó“ÕĶÓļ¹ ¾„Ķ“ÕļÕķ ╬“ “ÕŅĶĶ Ļ ’ÓĻ“ĶĻÕ (ŌĶõÕŅ) 90-ļÕ“ĶÕ ŅßÓńŅŌÓĒĶ ęÓ“Ó±ĻŅķ └ččą ŽÕ±ŅĒÓļĶĶ: ŽÕõ±ÕõÓ“ÕļĶ ’ÓŌĶ“Õļ³±“ŌÓ ŽÕ±ŅĒÓļĶĶ: ═ÓĻŅņ’Ņ±¹ ŽÕ±ŅĒÓļĶĶ: ┬¹õÓ■∙ĶÕ± õÕ “ÕļĶ Ķ±“ŅĶĶ “Ó“Ó±ĻŅŃŅ ĒÓŅõÓ šš Ō. ŽÕ±ŅĒÓļĶĶ: ŽÕõ±ÕõÓ“ÕļĶ ęÓ“ų╚╩Ó Ķ ŽÕńĶõĶ¾ņÓ ┬Õ§ŅŌĒŅŃŅ čŅŌÕ“Ó ę└ččą ŽÕ±ŅĒÓļĶĶ: ŽÕŌ¹Õ ±ÕĻÕ“ÓĶ ęÓ“Ó±ĻŅŃŅ ŅßĻŅņÓ, Õ±ĻŅņÓ ’Ó“ĶĶ ╚±“ŅĶ : Ņ¶Ķ÷ĶÓļ³Ē¹Õ õŅĻ¾ņÕĒ“¹ ┬Õ§Ķ Ķ±“ŅĶĶ šŅĒĶĻÓ Ķ±“ŅĶĶ ę└ččą įŅ“ŅŃÓ¶ĶĶ ŽŅ¶Ķļ³ĒŅÕ Ņß¾„ÕĒĶÕ Ō ±ÕõĒÕķ °ĻŅļÕ čŅõÕµÓĒĶÕ Ķ ±Ņ’ŅŌŅµõÕĒĶÕ ═ŅņÓ“ĶŌĒŅÕ ŅßÕ±’Õ„ÕĒĶÕ įŅņ¹ Ķ“ŅŃŅŌŅķ Ó““Õ±“Ó÷ĶĶ ╠ÕŅ’Ķ “Ķ įŅ¾ņ¹ 2010 ąÓ±’Ķ±ÓĒĶÕ ¶Ņ¾ņŅŌ ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ņÓ“ÕņÓ“ĶĻÕ ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ¾±±ĻŅņ¾ ń¹Ļ¾ ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ßĶŅļŅŃĶĶ Ķ §ĶņĶĶ ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ¶ĶńĶĻÕ (16 - 17 ¶ÕŌÓļ 2010 Ń.) ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ĶĒŅ±“ÓĒĒ¹ņ ń¹ĻÓņ (25 - 26 ¶ÕŌÓļ 2010 Ń.) ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ĶĒ¶ŅņÓ“ĶĻÕ (2 - 3 ņÓ“Ó 2010 Ń.) ╚Ē“ÕĒÕ“-¶Ņ¾ņ ’Ņ ŃÕŅŃÓ¶ĶĶ (4 - 5 ņÓ“Ó 2010 Ń.) Ų¾ĒÓļ "╚Ē¶ŅņÓ“ĶńÓ÷Ķ ŅßÓńŅŌÓĒĶ . ŽŅßļÕņ¹ Ķ ’ŅĶ±ĻĶ" č“Ó“³Ķ µ¾ĒÓļÓ "╚Ē¶ŅņÓ“ĶńÓ÷Ķ ŅßÓńŅŌÓĒĶ . ŽŅßļÕņ¹ Ķ ’ŅĶ±ĻĶ" Ž¾ßļĶ„Ē¹Õ ļÕĻ÷ĶĶ ╬ß∙Ó ĶĒ¶ŅņÓ÷Ķ 2007/2008 2008/2009 2009/2010 III Ņ“Ļ¹“¹ķ ĻŅĒĻ¾± ĶĒ“ÕĒÕ“ ±Óķ“ŅŌ čÓķ“¹-¾„Ó±“ĒĶĻĶ ŽĶĻÓń Ņ ’ŅŌÕõÕĒĶĶ ╠ÕŅ’Ķ “Ķ ąÕ±’¾ßļĶĻÓĒ±ĻŅÕ ÓŌŃ¾±“ŅŌ±ĻŅÕ ±ŅŌÕ∙ÓĒĶÕ ÓßŅ“ĒĶĻŅŌ ŅßÓńŅŌÓĒĶ Ķ ĒÓ¾ĻĶ 2009 IV ąÕ±’¾ßļĶĻÓĒ±ĻĶķ ╚Ē“ÕĒÕ“-’Õõ±ŅŌÕ“ IV ąÕ±’¾ßļĶĻÓĒ±ĻŅķ ĶĒ“ÕĒÕ“-ÓĻ÷Ķ "═ÕõÕļ ŅßÓńŅŌÓĒĶ ŌńŅ±ļ¹§" ╚Ē¶ŅņÓ÷Ķ Ņ ĒÕõÕļÕ ŅßÓńŅŌÓĒĶ ŌńŅ±ļ¹§ ŽŅŌ¹°ÕĒĶÕ ĻŌÓļĶ¶ĶĻÓ÷ĶĶ ’Ņ ╚╩ę ═Ņ¾“ß¾Ļ ¾„Ķ“Õļ . ╬±ĒŅŌ¹ ÓßŅ“¹ ŽŅŃÓņņÓ Intel "╬ß¾„ÕĒĶÕ õļ ß¾õ¾∙ÕŃŅ" ŽŅŃÓņņÓ "ė„Ķņ± ± Intel" ╩ÓļÕķõŅ±ĻŅ’ 

|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|